目的 研究根管治疗过程中次氯酸钠(sodium hypochlorite,NaOCl)冲洗溶液对牙本质粘接强度的影响。方法 选取新鲜拔除的人第三磨牙15颗,牙冠完整无龋坏,未经牙体或牙髓治疗,去除釉质,暴露中层牙本质,600目砂纸打磨牙本质表面1 min,去离子水冲洗1 min,制备牙本质平面试件。试件随机分为3组,采用不同表面处理方法后制作粘接试件:A组(阴性对照组),去离子水处理牙本质平面试件20 min;B组(2.50% NaOCl实验组),2.50% NaOCl溶液处理牙本质平面试件20 min,每5分钟更换1次新鲜溶液;C组(5.25% NaOCl实验组), 5.25% NaOCl溶液处理牙本质平面试件20 min,每5分钟更换1次新鲜溶液。处理后所有试件表面均使用自酸蚀粘接剂SE bond进行粘接处理,上方堆塑5 mm高的AP-X复合树脂,分层固化后,粘接试件置于37 ℃去离子水中储存24 h后,使用金刚石切割机垂直于粘接界面切割,制作1.0 mm×1.0 mm条状试样( n=45)。用微拉伸测试仪测试条状试样微拉伸粘接强度(MPa), 体视显微镜下观察试样断裂类型(界面破坏、内聚破坏及混合破坏类型),采用单因素方差分析比较不同实验组的微拉伸粘接强度,并用Post-hoc test(LSD)法进行两两比较,应用卡方检验比较不同组之间断裂类型分布的差异,并进行两两比较。结果 2.50%NaOCl实验组[(26.04±5.74 )MPa]和5.25%NaOCl实验组[(24.46±3.77) MPa]的粘接强度明显低于未经NaOCl溶液处理的阴性对照组[(48.71±7.77 )MPa], P=0.000。与阴性对照组比较,2.50%和5.25%NaOCl实验组粘接强度分别下降了46.5%和50.2%,2.50%和5.25%NaOCl实验组间粘接强度差异无统计学意义( P=0.214)。不同实验组之间断裂类型分布差异均具有统计学意义( χ2=56.324, P=0.000), 阴性对照组试样断裂类型以混合破坏类型(68.9%)为主,界面破坏类型(24.4%)次之,内聚破坏类型(6.7%)最少,2.50%NaOCl实验组与5.25%NaOCl实验组发生界面破坏类型的比例明显高于阴性对照组( P=0.000),2.50%NaOCl实验组和5.25%NaOCl实验组间的断裂类型分布差异无统计学意义( P=0.197),且均未发现内聚破坏。结论 NaOCl处理过的牙本质与复合树脂的粘接强度明显降低。
Objective: To evaluate the influence of sodium hypochlorite (NaOCl) solution used during root canal therapy on dentin bond strength.Methods: In the study, 15 freshly extracted human third molars with complete dental crowns, caries and filling-free were selected. The occlusal enamel was removed perpendicular to the long axis of the tooth to expose middle flat surfaces of sound dentin. The occlusal dentin surfaces were then polished using 600-grit silicon papers for 1 min and rinsed with deio-nized water for 1 min. The teeth were randomly divided into three groups according to the treatment received: group A (negative control group), the samples were immersed in deionized water for 20 min; group B, the dentin surfaces were immersed in 2.50% NaOCl solution for 20 min, with the solution being renewed every 5 min; group C, the dentin surfaces were immersed in 5.25% NaOCl solution for 20 min, with the solution being renewed every 5 min. All the treated dentin surfaces were bonded using a self-etching adhesive system (SE bond) with a 5 mm in height resin composite (AP-X). After storage in deionized water at 37 ℃ for 24 h, the adhesive samples were sectioned longitudinally to produce 1.0 mm×1.0 mm stick specimens( n=45) for micro-tensile bond strength testing (MPa). Failure modes (adhesive failure, cohesive failure or mixed failure) at the dentin-resin interface were observed using a stereomicroscope. The micro-tensile bond strength data among the three groups were analyzed by a one-way ANOVA, then the Post-hoc test(LSD)was employed for pairwise comparison. The distribution of failure modes among the groups were analyzed by chi square test.Results: Significant decreased bond strength values were found for the 2.50% NaOCl-treated group (26.04±5.74) MPa and 5.25% NaOCl-treated group (24.46±3.77) MPa when compared with the strength of negative control group (48.71±7.77) MPa, P=0.000. Compared with the negative control group, themicro-tensile bond strength of the 2.50% NaOCl-treated group and 5.25% NaOCl-treated grouphad dropped by 46.5% and 50.2%. However, there was no significant difference of bond strength between the 2 NaOCl-treated groups ( P=0.214). The distribution of failure modes showed significant difference in all the three groups (2=56.324, P=0.000). The mixed failure (68.9%) was the most mode of fracture in the negative control group, followed by adhesive failure(24.4%), and the cohesive failure was least(6.7%). The proportion of adhesive failure mode was higher in NaOCl-treated groups than in negative control group ( P=0.000). There was no significant difference of the distribution of failure modes between the 2.50% NaOCl-treated group and 5.25% NaOCl-treated group( P=0.197), and there was no cohesive failure mode detected in the two groups.Conclusion: The micro-tensile bond strength of dentin to composite resin was lower after exposure to NaOCl solution.
次氯酸钠(sodium hypochlorite, NaOCl)是临床使用最广泛的根管冲洗液, 具有很强的杀菌能力, 可以杀灭根管系统内及根管壁上定植的微生物, 中和细菌产生的毒素, 还可以溶解生活或坏死牙髓组织, 且能在根管预备过程中起到润滑作用[1]。
近年来随着材料与技术的发展, 使用复合树脂进行根管治疗后即刻粘接修复应用越来越广泛。即刻粘接修复可以有效防止冠方渗漏, 冠方严密封闭依赖于牙本质与修复材料间形成良好的粘接, 有效的粘接可以防止修复体与牙体组织间边缘微渗漏、修复体脱落等[2]。
但是, 研究者也注意到NaOCl溶液在发挥杀菌、溶解组织等作用的同时, 可能会对牙本质理化性能产生影响。已有研究证实, NaOCl溶液处理后的牙本质, 其微硬度[3]、弹性模量和挠曲强度[4]均有所降低, 由此, NaOCl溶液是否会改变牙本质的粘接强度也引起临床医生与学者的关注。目前关于NaOCl溶液对牙本质粘接强度影响的研究较少, 在不同的研究中采用的NaOCl溶液的浓度剂型、处理时间和方法不一, 结论并不一致。
本研究旨在探讨不同浓度 NaOCl溶液对牙本质粘接强度的影响, 以期为临床提供参考。
离体牙的选择:选取新鲜拔除的第三磨牙15颗, 浸泡于去离子水中, 牙冠完整无龋坏, 未经牙体或牙髓治疗, 用手用刮治器械去净表面残留软组织及牙结石, 4 ℃下储存于去离子水中, 3个月内使用。
离体牙包埋与去釉:将离体牙用自凝树脂(Heraeus Kulzer公司, 德国)包埋, 使用金刚石切割机(SYJ-150, 沈阳科晶自动化设备有限公司, 中国), 在水冷却下去除釉质, 暴露中层牙本质, 体视显微镜(20倍, Zoom630, 上海长方光学仪器有限公司)下检查确认已去净釉质。之后用600目砂纸湿性打磨牙本质表面1 min, 去离子水冲洗1 min, 制备成牙本质平面试件。
分组:将15个离体牙试件随机分为3组, 每组5个, 按照表面处理方式不同分为:A组(阴性对照组), 试件浸泡于去离子水中20 min; B组, 2.50% (体积分数)NaOCl溶液浸泡试件20 min(每5 min更换1次新鲜溶液); C组:5.25%(体积分数) NaOCl溶液浸泡试件20 min(每5分钟更换1次新鲜溶液)。
涂布粘接剂:按照说明书要求, 使用毛刷轻力双向涂擦, 将两步法自酸蚀粘接系统SE Bond(Kuraray公司, 日本)涂于待粘接面, 操作步骤为:中等气流轻吹, 干燥牙面; 涂粘接预处理剂, 静置20 s; 中等强度气流彻底干燥; 涂粘合剂, 轻吹使分布均匀; 光固化10 s。吹干粘接剂时, 气枪与待粘接面呈45° 角, 约保持1 cm距离, 气流大小一致。
充填树脂:粘接剂使用之后, 将复合树脂AP-X(Kuraray公司, 日本)分层堆砌于粘接面上形成约5 mm高树脂块, 每层厚度< 2 mm, 用光固化灯(LEDition, Ivoclar Vivadent公司, 列支敦士登公国)固化20 s, 光强度800 mW/cm2。将制备好的粘接试件即刻储存于去离子水中, 置于电热恒温水槽(上海森信实验仪器有限公司)37 ℃恒温保存24 h后进行微拉伸实验。
使用金刚石切割机(SYJ-150, 沈阳科晶自动化设备公司, 中国), 水冷却下垂直于粘接界面将试件切割成1 mm厚的片状, 试件旋转90° , 再次纵向切割, 得到约1.0 mm× 1.0 mm的条状试样。
每个粘接试件经切割得到20~30个条状试样, 在体视显微镜(20倍, Zoom630, 上海长方光学仪器有限公司)下观察, 排除有气泡、裂纹、缺损的缺陷试样, 筛选出 8~12个条状试样备用, 每组5个粘接试件得到45个条状试样(n=45), 进行微拉伸粘接强度测试(图1)。用游标卡尺(MNT-150, 上海迎特贸易有限公司)测量每个试样截面的长度(a)和宽度(b), 粘接面积S(mm2)=a× b, 然后使用氰基丙烯酸粘接剂(广东爱必达胶粘剂有限公司)将试样两端固定在微拉伸测试仪(MicroTensile Tester, Bisco公司, 美国)试样台上, 使长轴与试样台平行且粘接面位于试样台正中。启动测试仪, 速度1 mm/min, 直至样本断裂, 记录断裂时拉力峰值F(N), 计算微拉伸粘接强度(MPa)=F/S。
 | 图1 微拉伸粘接强度测试试样制备示意图Figure 1 Schematic illustration of sample preparation for microtensile bond strength testing |
断裂类型分析:体视显微镜(45倍, Zoom630, 上海长方光学仪器有限公司)下观察并记录试件断裂破坏类型, 分为界面破坏、内聚破坏及混合破坏3种, 内聚破坏又可以分为牙本质内聚破坏和复合树脂内聚破坏(图2)。
采用SPSS 20.0统计软件(IBM公司, 美国)对所测得的各组试样微拉伸强度值进行统计学分析, 计算均数± 标准差。采用单因素方差分析(one-way ANOVA)检验各组试样微拉伸强度值间的差异, 并用Post-hoc test(LSD)法进行两两比较, 检验水准为双侧α =0.05。断裂类型分布的比较采用卡方检验, 检验水准为双侧α =0.05, 两组之间的比较用Bonferroni方法校正检验水准(α =0.017)。
阴性对照组、2.50%NaOCl实验组、5.25%NaOCl实验组(n=45)的平均微拉伸粘接强度分别为(48.71± 7.77)Mpa、(26.04± 5.74)MPa、(24.46± 3.77) MPa。3个实验组之间粘接强度差异有统计学意义(F=230.941, P=0.000), 其中, 2.50%NaOCl实验组与5.25%NaOCl实验组的粘接强度较阴性对照组显著降低(P=0.000), 分别比阴性对照组下降了46.5%和50.2%, 5.25%NaOCl实验组的粘接强度低于2.50%NaOCl实验组, 但两组间差异无统计学意义(P=0.214)。
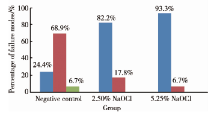
各组断裂类型分布见图3。3个实验组之间断裂类型分布不同(χ 2=56.324, P=0.000), 阴性对照组(n=45)试样断裂类型以混合破坏类型(68.9%)为主, 界面破坏类型(24.4%)次之, 内聚破坏类型(6.7%)最少; 2.50%NaOCl实验组(n=45)与5.25%NaOCl实验组(n=45)发生界面破坏类型的比例明显高于阴性对照组(P=0.000); 2.50%NaOCl实验组和5.25%NaOCl实验组间的断裂类型分布差异无统计学意义(P=0.197), 且均未发现内聚破坏。
牙本质粘接强度的研究方法包括传统拉伸实验、微拉伸实验、微剪切实验等, 本研究采用微拉伸实验方法评价次氯酸钠处理后的牙本质粘接强度。微拉伸实验是Sano等[5]于1994年提出的, 通过测定试件在承受负荷发生断裂时的微拉伸强度来评价材料的粘接强度。与传统拉伸实验和微剪切实验相比, 微拉伸实验可以测试很小面积的粘接强度, 减少了界面内缺陷的干扰, 应力分布更均匀, 还可以通过制作多个试样, 测试牙齿不同部位的粘接强度, 粘接面积小, 便于扫描电镜观察[6]。综合考虑以上因素, 微拉伸实验为目前较为合适的也是应用最广泛的评估牙本质与材料之间的粘接强度的研究方法, 因此本研究选取微拉伸实验作为主要实验方法。
微拉伸实验结果也会受到试样几何形状、试样粘接面积、测试速度等因素的影响, 本研究选择试样类型为条状试样, 制备过程简单, 可以避免试样修整过程产生额外应力[7]。已有研究证明, 在0.5~2 mm2范围内试样粘接面积越小, 内部缺陷越少, 应力分布越均匀[7], 但是粘接面积小于1 mm2时, 容易在制备过程中出现试样折断[8], 因此本研究中采用的试样粘接面积为1 mm2, 以保证结果稳定可靠。此外, 实验过程中拉伸速度过快或过慢, 都可能导致应力不均匀, 影响测试结果的准确性, 有研究者推荐合适的拉伸速度为1 mm/min[7], 与本研究测试速度一致。
本研究中未经NaOCl溶液处理的阴性对照组的微拉伸粘接强度为(48.71± 7.77 )MPa, 与其他类似研究结果接近, Ramos等[9]测试1 mm× 1 mm条状试样 (SE Bond), 其阴性对照组的粘接强度为(54.7± 7.8) MPa, 这也从另外一个侧面证实本研究实验技术的稳定性和可靠性。
本研究中, 2.50%NaOCl实验组与5.25%NaOCl实验组的粘接强度均明显低于阴性对照组, 分别比阴性对照组下降了46.5%和50.2%(P=0.000), 两个NaOCl实验组间粘接强度无差别(P=0.214)。亦有其他研究[10, 11, 12, 13, 14]证实了这一点, Barutcigil等[10]通过微拉伸实验测试5% NaOCl溶液处理5 min后的髓室侧壁牙本质, 其条状试样面积为1 mm× 1 mm, 拉伸速度为1 mm/min, 发现其粘接强度比对照组下降了56%。已有一些学者推测NaOCl溶液处理后牙本质粘接强度下降的原因可能为(图4):NaOCl使牙本质胶原蛋白分解, 影响混合层的形成, 粘接剂不能有效地渗入胶原纤维网和牙本质小管内[15]; 此外, NaOCl发生氯化反应生成的氧化自由基与甲基丙烯酸酯类单体聚合反应过程中产生的单体自由基反应, 也可以与粘接体系中的引发剂和自由基发生反应, 导致增长链自由基浓度下降, 产生过早的链终止, 从而影响粘接过程中的聚合反应[16]。综上所述, 牙本质胶原蛋白的分解以及氧化自由基的形成, 可能是导致NaOCl溶液处理后的牙本质粘接强度下降的直接原因。针对NaOCl溶液处理牙本质后粘接强度下降的问题, 一些研究者建议使用一些化学药物如抗坏血酸钠、硫代硫酸钠等处理粘接面, 以促进恢复牙本质粘接强度[11, 17], 但迄今尚无一致结论, 有待进一步深入研究。
也有研究者发现NaOCl处理过的牙本质粘接强度无变化甚至增高, Taniguchi等[18]发现6% NaOCl溶液处理牙本质15 s后, 牙本质微拉伸粘接强度无明显改变; Kambara等[19]通过剪切试验测试1% NaOCl溶液处理15 s后的牙本质粘接强度, 牙本质与复合树脂的粘接强度甚至有明显提高。分析与本实验结果不同的原因可能为:上述两篇文献中, 处理时间均为15 s, 本研究所设定的处理时间为20 min; 在Kambara等[19]的研究中, NaOCl溶液浓度仅为1%, 本研究浓度设置为2.50%和5.25%, 处理时间和处理浓度的差异可能是造成研究结果不同的重要原因。本研究NaOCl溶液浓度(2.50%、5.25%)以及处理时间(20 min)是考虑临床根管预备的实际条件而设置, 与临床条件更为接近。
本实验中阴性对照组的试样断裂类型以混合破坏类型居多, 即断裂同时发生在粘接界面及被粘接物内部, 表明粘接力与内聚力大致相等, 体现了材料、粘接剂、牙本质间的“ 一体化” 。Giannini等[20]也发现了类似的结果:制备长轴与牙本质小管方向平行的条状试样, 测试其抗拉强度, 发现中层牙本质的极限拉伸强度(ultimate tensile strength, UTS)为(48.7± 16.6)MPa, 与本实验测得的牙本质与复合树脂间微拉伸强度平均值(48.71± 7.77 )MPa接近, 而经NaOCl处理后的牙本质, 界面破坏类型比例明显提高, 即断裂发生在粘接界面上, 该结果说明NaOCl溶液处理后在试件粘接界面出现 “ 相对薄弱区” , 也从另一个侧面反映了NaOCl溶液处理后牙本质粘接强度的降低。此外, 本实验135个条状试样中只有3个发生了内聚破坏, 其余均为界面破坏或混合破坏。
综上所述, 在本实验的条件下, 2.50%和 5.25% NaOCl溶液处理过的牙本质, 其与复合树脂的粘接强度明显降低, 且粘接界面成为相对薄弱区, 界面断裂明显增多。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|