目的 评估超声造影引导肾穿刺建立工作通道用于经皮肾镜取石术的有效性。方法 该回顾性研究纳入20例在北京大学第一医院诊断为肾结石的患者,患者的人口学基线数据、临床特点、手术治疗以及术后情况来自于北京大学第一医院综合病例数据库。全身麻醉后在超声造影技术实时监控下由同一泌尿外科医师进行经皮肾穿刺,再利用钬激光或气压弹道进行碎石,记录患者的基线临床资料、结石特征以及手术过程,最后,利用统计学分析方法评价超声造影引导经皮肾穿刺用于经皮肾镜取石术的安全性和有效性。结果 20例患者均在超声造影引导下成功行肾穿刺建立工作通道,并完成经皮肾镜取石手术。所有患者均成功穿刺入肾集合系统并建立良好的工作通道,仅1例患者接受了二次肾穿刺,并且所有患者均为通过肾中盏穿刺。中位穿刺时间3.9 min(四分位数:2.9~4.6 min),而中位手术时间是112 min(四分位数:98.5~134.5 min)。术后48 h的泌尿系平片 (kidney ureter bladder, KUB) 显示初步结石清除率为95.0%(19/20),而中位血红蛋白下降水平为10 g/L (四分位数:5.5~14.5 g/L)。2位患者术后出现暂时性发热,并且对抗生素反应良好,除此之外,无其他严重并发症出现。结论 对于处在经皮肾镜取石术手术学习曲线中的泌尿外科医师,使用注射用六氟化硫微泡超声造影引导经皮肾穿刺建立工作通道是一种安全且有效的方法。该技术使肾穿刺过程更加可视化且简单化,可获得相比于普通超声更为清晰的高质量图像。经皮肾镜取石术初学者可能从该项技术中获益从而缩短学习曲线,但是这需要进一步的前瞻性对比研究加以明确和证实。
Objective: Contrast enhanced ultrasound (CEUS) is an innovative technique that employs microbubble contrast agents to demonstrate parenchymal perfusion. Ultrasound contrast agent was reported to be directly used in human internal lumen to improve the observation capacity of ultrasound. However, CEUS has never been reported to be used in the guidance of percutaneous renal access in percutaneous nephrolithotomy (PCNL). This study aimed to assess the efficacy of CEUS-guided renal access in PCNL.Methods: In this retrospective study, percutaneous renal access was performed under real-time monitoring of CEUS during PCNL in a cohort of 20 patients with renal stones at Peking University First Hospital. Data regarding patients’ demographic and clinical characteristics, therapeutic regimens, and postoperative information were collected from a comprehensive database containing comprehensive medical records of the patients undergoing PCNL. Briefly, the procedure was as follows. With the patient under general anesthesia, renal access was established by the guidance of CEUS. Afterwords, holmium laser, pneumatic or ultrasonic lithotripsy was used by the same urologist. The patient demographics, stone characteristics and procedure details were noted. Finally, appropriate statistical analyses were performed to evaluate the effectiveness and safety of the CEUS-guided percutaneous renal access in PCNL.Results: All the 20 patients underwent PCNL successfully with the help of CEUS guidance for tract creation. The collecting system was successfully accessed in all the patients, and only one patient underwent re-puncture. All the patients approached through a middle-pole percutaneous access. The median puncture time was 3.9 (2.9-4.6) min, and the median operating time was 112 (98.5-134.5) min. The preliminary stone-free rate of PCNL was 95.0% (19/20) as shown by the kidney, ureter, and bladder (KUB) radiographs 48 h postoperation, and the median decline in hemoglobin level was 10 (5.5-14.5) g/L. Two patients had transient postoperative fever and responded well to antibiotics. In addition, no other major complications were observed.Conclusion: CEUS is a safe and effective alternative way of guidance for percuta-neous renal access for PCNL beginners. It makes this procedure more visualized and simpler, and produces clearer images than common ultrasonic ones. PCNL beginners might benefit from this method to shorten the learning curve of PCNL, while it warrants further comparative studies to clarify.
经皮肾镜取石术(percutaneous nephrolithotomy, PCNL)已被公认为是针对大于2 cm的肾结石或鹿角形结石的首选治疗方案[1]。在经皮肾镜取石手术的过程中, 首次肾穿刺即成功建立工作通道至关重要, 因为这有助于减少并发症发生率, 并且提高结石清除率。经皮肾穿刺需要影像学技术的帮助, 例如X线透视或超声[2]。X线透视引导下经皮肾穿刺具有较高的准确性和成功率, 此方法在美国应用广泛[3], 但是它对患者和医务工作者都可能产生潜在的健康危害, 因为此过程无法完全避免射线暴露[4]。再者, 肾的邻近器官(例如结肠、肝和肺)在X线透视下无法显示, 故副损伤的发生率可能较高。在亚洲国家(尤其是中国), 超声引导下肾穿刺被广泛应用, 它使患者和医务人员不受射线暴露的不良影响[5, 6]。另外, 超声可实时观察肾与周围器官, 降低周围内脏副损伤的风险。超声引导下肾穿刺应用于经皮肾镜取石术的有效性及安全性已被以往多项研究证实[7], 但在某些情况下, 例如无明显肾积水、合并肾盂旁囊肿、肾纤维化以及肥胖等, 仅通过超声技术定位肾盂肾盏的难度增加。既往研究显示, 初学者需要积累超过60例PCNL手术中超声引导下经皮肾穿刺经验才能掌握该项技术[8, 9], 因此, 如何提高PCNL术中超声引导下经皮肾穿刺的可视性和准确性, 并缩短初学者的学习曲线则是一个亟待解决的问题。
超声造影技术是一种利用静脉注射微泡造影剂以显示实质器官灌注并且提高观察能力的新型技术, 其已被广泛应用于评价人体器官, 包括肝、前列腺以及肾[10, 11]。注射用六氟化硫微泡是一种二代微泡超声造影剂, 其含有高密度的惰性气体— — 六氟化硫[12]。六氟化硫直径约2.5 μ m, 具有良好的稳定性, 它能提高超声的回波率, 提高超声造影剂充盈区域与周围组织的对比度。注射用六氟化硫微泡的常见副作用程度一般较轻, 多为暂时的并且具有自限性, 不会出现后遗症, 静脉使用时极少出现过敏反应。既往报道已证实, 注射用六氟化硫微泡是一种安全可靠的造影剂, 并已广泛地在临床上使用[13]。曾有研究已经证实了超声造影技术用于输卵管超声造影的安全性和有效性[14]。另一项针对小儿患者的研究亦证实了在膀胱内使用注射用六氟化硫微泡行超声造影用于诊断膀胱输尿管反流性疾病的良好安全性[15], 因此, 该研究尝试利用超声造影剂逆行肾盂造影改善PCNL术中肾集合系统显像情况, 有利于经皮肾穿刺建立工作通道。
该回顾性研究纳入在北京大学第一医院泌尿外科诊断为肾结石并接受超声造影引导经皮肾穿刺的PCNL手术的20例患者。纳入标准:肾盂或肾盏结石直径> 2.0 cm, 或多发肾结石, 或鹿角形结石。所有患者接受常规术前检查, 并行CT检查评估术前肾结石位置和大小。结石大小的评估主要是测量患者术前CT显示的结石最大径长度。另外, 所有手术均由同一位泌尿外科医师完成。该项研究已通过北京大学第一医院医学伦理委员会批准, 并且在术前所有患者均签署知情同意书。
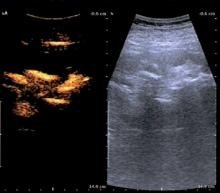
具体手术过程如下:在全身麻醉和预防性使用抗生素后, 患者处于截石位时逆行插入5 F(1 F=0.133 mm)型号的输尿管导管(莱凯公司, 德国), 其上端位置需到达肾盂或输尿管近端, 并将其与导尿管固定。然后患者改俯卧位进行后续的手术操作。超声影像处理系统采用的是B-K Medical Pro Focus 2202, 超声探头为ultrasonic probe 8823 (1.8~6.0 MHz)。由于肾及其周围组织和穿刺针在B模式下的图像质量通常优于超声造影模式, 所以将屏幕设置为双图像显示模式(左侧:超声造影模式; 右侧:B模式)。超声造影剂采用注射用六氟化硫微泡(博莱科公司, 意大利), 使用时以59 mg注射用六氟化硫微泡与生理盐水充分混合并稀释至50 mL。在超声造影模式的实时监控下, 通过先前放置好的输尿管导管向肾盂和肾盏内注入10 mL已稀释的注射用六氟化硫微泡, 然后调整超声探头来观察集合系统的形态。在超声造影模式下, 整个集合系统(包括扩张积水不明显的肾盂肾盏)显影的影像质量明显优于B模式(图1)。然后, 所有患者均在超声造影模式的实时监控下确定合适的穿刺点和穿刺方向, 再徒手进行肾盏穿刺。因为在超声造影模式下穿刺针无法清楚显示, 故需要在B模式下确认穿刺方向和深度。完成穿刺后拔出针芯, 通过输尿管导管再注入10 mL已稀释的注射用六氟化硫微泡, 在超声造影模式下可见超声造影剂流入穿刺针则提示穿刺成功。再通过穿刺针向肾集合系统插入斑马导丝(波士顿科学公司, 美国)。根据结石的大小和碎石的具体方式, 借助导丝用肾穿刺套装(莱凯公司, 德国)将工作通道扩张至18~24 F。最后, 向已扩张的工作通道内置入可剥脱鞘(库克医疗公司, 美国), 根据具体情况插入8/9.8 F硬输尿管镜(狼牌公司, 德国)联合钬激光碎石(科医人公司, 美国)或插入标准20 F肾镜(奥林巴斯公司, 日本)联合气压弹道碎石(电子医疗系统公司, 瑞士)进行碎石。
详细记录整个手术过程中穿刺次数、穿刺时间、手术时间和手术相关并发症情况。所有患者术后第一天早晨复查血常规评价血红蛋白水平变化程度, 并在术后48 h进行泌尿系平片(kidney ureter bladder, KUB)评估结石清除率。鉴于所有结石均为不透光结石, 故结石完全清除被定义为术后KUB提示所有结石碎片最大径均≤ 4 mm。
所用数据均被录入SPSS 20.0统计学分析软件, 除非特别注明, 数据表示形式均为中位数(四分位数)或例数。
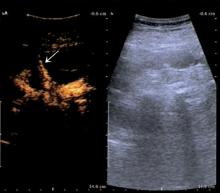
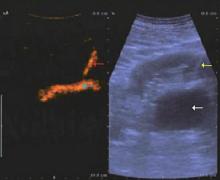
总共20例肾结石患者在完善常规术前检查后接受该手术方式。表1所示的是患者基线临床数据, 表2所示的是患者手术过程详细信息。在所有患者中均成功穿刺入肾集合系统并建立良好的工作通道, 仅1例患者接受了二次肾穿刺, 并且所有患者均为通过肾中盏穿刺。从开始穿刺到成功建立工作通道的中位时间为3.9 min(2.9~4.6 min), 中位手术时间为112 min(98.5~134.5 min)。PCNL术后48 h行KUB评估的结石清除率为95.0%(19/20), 中位血红蛋白降低值为10 g/L(5.5~14.5 g/L)。2例患者出现一过性术后发热, 并对抗生素治疗反应良好。其他严重并发症, 如动静脉瘘、结肠损伤、气胸、胸腔积液或氮质血症均未出现。最后, 图1所示的是超声造影技术下肾集合系统显影, 相比于B模式具有更好的可视性和图像锐度, 而图2所示的是超声造影模式图像显示超声造影剂流入穿刺针提示经皮肾穿刺成功。另外如图3所示, 有1例患者合并肾盂旁囊肿, 我们利用超声造影技术引导肾穿刺可清楚显示集合系统的位置和结构, 避免穿入肾盂旁囊肿。
| 表1 患者基线临床资料 Table 1 Patients’ baseline clinical features |
| 表2 手术详细情况 Table 2 Procedure details |
该研究报道超声造影技术应用于引导PCNL手术中经皮肾穿刺建立工作通道, 经皮肾穿刺建立工作通道是PCNL手术中至关重要的一步, 需要其具备安全、有效并稳定的特点。为建立一个理想的工作通道, 我们应该关注以下几个关键点:第一, 选择合适的肾盏进行穿刺, 以便触及并清除所有结石; 第二, 经过肾盏穹窿部穿刺进入肾集合系统, 这样可以避免损伤盏颈周围的血管, 降低术中及术后的出血风险; 第三, 沿肾盏至盏颈的轴向方向插入穿刺针, 从而维持工作通道的稳定性, 并且可降低在扩张通道和碎石过程中通道丢失的发生率。
超声引导下经皮肾穿刺具备一些优势, 例如不暴露于射线、易于调整并可实时观察临近器官避免内脏损伤。但是, 超声引导下经皮肾穿刺的学习曲线相对较长, 初学者需要接受较长时间的专业培训方能掌握该项技术。与X线透视相比, 超声的可视性较差, 难以清楚地显示整个肾集合系统, 这导致选择最佳肾盏进行穿刺的难度增加。在肾积水扩张不显著、合并肾盂旁囊肿、肾盏盏颈狭窄以及肥胖等情况下, 超声引导下建立工作通道的难度显著增加, 故可能导致包括出血在内的并发症发生率升高。
输卵管造影术是一种通过直接向子宫宫腔内注入超声造影剂从而使输卵管结构显影的检查手段。据既往研究报道, 输尿管造影术可帮助避免放射性损伤和传统检查引起的不适或疼痛, 并且副作用少, 使其成为一种安全、有效、广泛应用于评估输尿管通畅程度的方法[16]。另外, 据报道在经皮经肝胆道引流术中, 注射用六氟化硫微泡可通过引流导管直接注射入胆道, 从而提高引流导管的可视性, 并可评估胆道梗阻水平和程度[17]。由此可见, 超声造影剂可直接用于人体内腔道来提高超声的观察能力。
使用注射用六氟化硫微泡行超声造影让经皮肾穿刺过程更加可视化且简单化, 穿刺点定位及穿刺方向把握更加准确。因为超声造影可获得与X线造影显像类似的肾集合系统图像, 有助于全面地观察肾集合系统结构, 故可快速定位理想的肾盏, 进而准确地决定穿刺进针点和进针方向。完成肾穿刺后, 亦可通过超声造影清楚地观察穿刺针进入肾集合系统的位置以及穿刺针与肾盏至盏颈轴线之间的角度, 借此评价穿刺质量, 代替了通过水从穿刺针流出情况来评价的方式。因为超声造影技术的直观性, 初学者更容易理解并掌握经皮肾穿刺技术, 并降低相关并发症的发病率。
但是, 该研究和此项新技术仍存在一些不容忽视并有待改善的限制和缺陷。首先, 对于严重肾积水的患者, 因为肾盂肾盏扩张体积较大, 造成造影剂注入量相对较少, 最终导致超声造影图像质量较差。对于该类患者, 超声造影引导肾穿刺相比于普通超声并无显著优势, 但是可用于该类患者因初次穿刺失败而导致肾积水不显著的情况。其次, 因为穿刺针在B模式下图像相比于超声造影模式更为清晰, 故手术中需同时开启B模式和超声造影模式, 因此, 希望可改进超声造影模式或设计生产新型超声设备, 使仅在超声造影模式下即可清楚观察肾集合系统和穿刺针情况。再者, 该研究中进行该项手术操作的泌尿外科医师在该研究开始前已经具备普通超声引导PCNL中经皮肾穿刺的初步经验, 因此需要进一步的前瞻性和对照研究以评价超声造影引导对经皮肾穿刺临床价值, 尤其是明确其是否可缩短PCNL初学者经皮肾穿刺建立工作通道的学习曲线。
对于处在PCNL手术学习曲线中的泌尿外科医师, 使用注射用六氟化硫微泡行超声造影引导经皮肾穿刺建立工作通道是一种安全且有效的方法。该技术使肾穿刺过程更加可视化且简单化, 可获得相比于普通超声更为清晰的高质量图像。PCNL手术初学者可能从该项技术中获益从而缩短学习曲线, 但是这需要进一步的前瞻性对比研究加以明确和证实。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|