目的 分析Stanford B型主动脉夹层累及腹腔四分支血管灌注不良情况,探讨腔内修复术对腹腔四分支血管灌注的影响。方法 回顾性分析2015年9月至2016年3月收治并确诊为Stanford B型主动脉夹层的患者32例,男28例,平均年龄(52.9±9.6) 岁(32~70岁),收集患者的临床影像学资料及随访结果。基于Nagamine分支血管灌注不良细化分型,分析术前和术后主动脉CT血管造影(computed tomography angiography,CTA)影像资料,对灌注不良的腹腔四分支血管(腹腔干动脉、肠系膜上动脉、左肾动脉及右肾动脉)进行分类和统计学分析。结果 32例患者腹腔四分支血管共128支,其中86支分支血管(67.2%)属于Ⅰ类灌注不良,Ⅰ-a亚型占60.9%(78/128),Ⅰ-b亚型占0.8%(1/128),Ⅰ-c亚型占5.5%(7/128);14支分支血管(10.9%)属于Ⅱ类灌注不良,Ⅱ-a亚型占3.9%(5/128),Ⅱ-b-1亚型占3.9%(5/128),Ⅱ-b-2亚型占3.1%(4/128);16支分支血管(12.5%)属于Ⅲ类灌注不良,均为Ⅲ-a亚型(无Ⅲ-b和Ⅲ-c亚型);其余12支分支血管未受累。32例患者均完成了胸主动脉腔内修复术(thoracic endovascular aortic repair, TEVAR),手术成功率100%,术后平均随访4个月。术后复查CTA显示,14支(10.9%)属于“高危”灌注不良亚型(Ⅰ-b、Ⅰ-c和Ⅱ-b-2亚型)的分支血管中,13支(92.9%)灌注不良明显改善,其余1支的灌注亚型由Ⅰ-b转归为Ⅰ-c。结论 Stanford B型主动脉夹层累及腹腔四分支血管灌注明显受损所占的比例较低,TEVAR能有效改善分支血管的灌注不良状态,推广Nagamine分支血管灌注不良细化分型,对判断夹层受累分支血管灌注不良状况及指导是否分支血管腔内重建意义重大。
Objective: To evaluate the efficiency of thoracic endovascular aortic repair (TEVAR) in dealing with abdominal aortic branch malperfusion based on the analysis of aortic computed tomography angiography (CTA) images in pre- and post-TEVAR.Methods: Retrospective analysis from September 2015 to March 2016 in single institution to 32 patients, diagnosed as Stanford B aortic dissection with abdominal aortic branch malperfusion, CTA images in pre- and post-TEVAR were collected. Based on the aortic branch malperfusion pattern redefined by Nagamine, we identified and characterized branch malperfusion pattern for four abdominal aortic branches (celiac trunk, superior mesenteric artery, bilate-ral renal artery) in statistical analysis.Results: In the four abdominal aortic branches (total 128 branches), 86 branches (67.2%) expressed with Class Ⅰ patterns, in which subtype Ⅰ-b presented with 0.8%, subtype Ⅰ-c with 5.5%; 14 branches (10.9%) expressed with Class Ⅱ patterns, in which subtype Ⅱ-b-1 with 3.9%, subtype Ⅱ-b-2 with 3.1%; 16 branches (12.5%) expressed with Class Ⅲ patterns, all with subtype Ⅲ-a, no subtype Ⅲ-b and Ⅲ-c presented. The remaining 12 branches were normal. The 100% successful rate of TEVAR obtained in 32 patients performed. The mean following-up was 4 months. Aortic CTA showed that among the 14 “high-risk” abdominal aortic branch malperfusion, 13 (92.9%) with obvious branch malperfusion in post-TEVAR were observed to improve, and the remaining one branch malperfusion (7.1%) was observed to change from subtype Ⅰ-b to Ⅰ-c.Conclusion: Few ratios in abdominal aortic branches suffered with obvious malperfusion complicated by Stanford B aortic dissection. For branches with “high-risk” malperfusion pattern, optimal changes were observed in abdominal aortic branch without revascularization in post-TEVAR, as well other branches with non-“high-risk” pattern perfusion were mostly stable in post-TEVAR. It could be of profound benefit to extend branch malperfusion patterns redefined by Nagamine in clinical practice to assess aortic dissection and in further guide for revascularization or not.
主动脉分支血管灌注不良是主动脉夹层的严重并发症, 常因夹层累及腹腔分支血管, 造成分支血管夹层或受压而引起血流灌注不良, 导致腹腔脏器缺血坏死、肾衰竭等严重后果[1, 2]。胸主动脉腔内修复术(thoracic endovascular aortic repair, TEVAR)治疗Stanford B型主动脉夹层不仅能隔绝夹层破口, 而且能有效改善主动脉分支血管的血流灌注[3], 然而, 分支血管灌注不良的形式不同, TEVAR对分支血管的改善效果亦不同, 因此, 探讨TEVAR对主动脉分支血管灌注的改善效果, 对进一步指导分支血管腔内重建有重要临床意义。Gaxotte等[4]对主动脉夹层累及分支血管灌注不良进行了分型, 在此基础上Nagamine等[5]进一步细化并再定义了分支血管灌注不良分型。基于此细化分型, 本研究分析了从2015年9月至2016年3月收治的32例Stanford B型主动脉夹层患者TEVAR手术前、后主动脉腹腔四分支血管分型的转归情况, 现报道如下。
回顾性分析2015年9月至2016年3月收治的Stanford B型主动脉夹层患者32例(男28例), 平均年龄(52.9± 9.6)岁(32~70岁), 其中急性期(≤ 15天)20例(62.5%), 亚急性和慢性期(> 15天)12例(37.5%)。
术前主要临床表现:胸部疼痛31例(96.9%), 伴腹部不适5例(15.6%), 伴间歇性跛行3例(9.4%); 另1例(3.1%)无症状, 为体检偶然发现。既往史:合并高血压27例(84.8%), 高血脂4例(12.5%), 冠心病3例(9.4%), 糖尿病3例(9.4%), 脑梗塞2例(6.3%); 10年以上吸烟史21例(65.6%), 具体见表1。所有患者均经术前CT血管造影(computed tomography angiography, CTA)检查证实为Stanford B型主动脉夹层。
| 表1 32例患者一般临床资料 Table 1 Clinic information of 32 patients |
根据分支血管形态学和血流动力学改变, Nagamine等[5]将分支血管灌注不良分为3种类型(图1)。
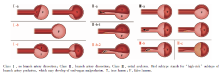 | 图1 Nagamine分支血管灌注不良的细化分型Figure 1 Branch artery perfusion in Stanford B aortic dissection by Nagamine |
Ⅰ 型:夹层未累及分支血管, 分支血管完全起自真腔, Ⅰ 型又分3种亚型。Ⅰ -a型:真腔未受假腔压迫, 分支血管血供良好; Ⅰ -b型:真腔受压塌陷导致分支血管血供受损; Ⅰ -c型:分支血管开口受内膜片影响导致血供受损。
Ⅱ 型:夹层累及分支血管。Ⅱ -a型:分支血管内存在较大再破口, 分支血管血供虽大部分来自假腔, 但血供良好; Ⅱ -b型:分支血管内无再破口或再破口较小, 分支血管供血大部分来自真腔。Ⅱ -b又分两型, Ⅱ -b-1型:分支血管内真腔不受假腔压迫, 分支血管血供好; Ⅱ -b-2型:分支血管内真腔受压, 分支血管血供受损。
Ⅲ 型:分支血管自开口处撕裂, Ⅲ 型又分3种亚型。Ⅲ -a型:分支血管血供大部分来自假腔, 合并或不合并分支血管夹层, 分支血管血供良好; Ⅲ -b型:分支血管内真腔受压, 分支血管血供受损; Ⅲ -c型:夹层假腔部分血栓化, 分支血管血供受损。
上述分型中, Ⅰ -b、Ⅰ -c、Ⅱ -b-2、Ⅲ -b和Ⅲ -c型由于分支血管血流灌注明显受损(内膜片撕裂入分支血管内或内膜片压迫真腔造成灌注不良)被定义为“ 高危(high-risk)” 亚型。本组病例中所有患者分支血管灌注不良亚型的判断均由两位专业影像医师分别阅片并汇总归类, 若两者意见不统一, 由上级医师阅片后决定。
32例患者中行急诊手术者3例(9.4%), 余为择期手术。所有病例均采用局部麻醉加强化麻醉。入路血管采用外科游离或预埋血管缝合器方式, 具体操作步骤依照我科常规操作方法[6, 7], 支架直径选择为近段锚定区直径(左锁骨下动脉后缘直径)的100%~120%(即oversize 0~20%)。基于夹层受累程度(真腔受压程度、假腔范围、是否迂曲成角), 53.1%的病例(17/32)选择了一条直筒型支架加一条大锥度支架(“ 两段式” )[8], 余病例采用一条直筒型支架。术中覆膜支架植入后即刻数字减影血管造影(digital subtraction angiography, DSA)评估分支血管灌注改善情况。对术前CTA影像显示“ 高危” 灌注不良的腹部四分支血管, 如TEVAR后分支血管灌注未改善, 同期行分支血管腔内重建术。对于术前存在下肢症状的患者, 结合术后DSA影像和检测股动脉搏动情况来评价下肢血管灌注恢复与否, 如无改变则拟行股动脉-股动脉转流手术。
收集患者术后1个月、6个月, 1年及以后每年1次主动脉CTA影像资料并进行分析(以本院CTA为主, 外院CTA为辅)。
所有数据采用SPSS 19.0 统计学软件进行相关统计学分析, 其中计量资料用均数± 标准差表示, 计数资料应用n (%)表示, 分类变量表示为占全部病例的百分比(%)。P≤ 0.05为差异有统计学意义。
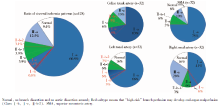
术前CTA和术中DSA评估腹主动脉四分支血管受累比例显示, 腹腔干动脉100.0%、肠系膜上动脉93.8%、左肾动脉84.0%、右肾动脉84.0%。基于Nagamine分支血管灌注不良分型, 本组32例患者四分支动脉(腹腔干动脉、肠系膜上动脉和双侧肾动脉)共128支, 其中86支分支血管(67.2%)属于Ⅰ 型(Ⅰ -a亚型占60.9%, Ⅰ -b亚型占0.8%, Ⅰ -c亚型占5.5%), 14支分支血管(10.9%)属于Ⅱ 型(Ⅱ -a亚型占3.9%, Ⅱ -b-1亚型占3.9%, Ⅱ -b-2亚型占3.1%), 16支分支血管(12.5%)属于Ⅲ 型(均为Ⅲ -a亚型, 无Ⅲ -b和Ⅲ -c亚型), 其余12支分支血管未受累(图2)。
分支血管受累灌注不良属于Ⅰ 型的比例:腹腔干动脉70%、肠系膜上动脉75%、左肾动脉75%、右肾动脉47%; 分支血管受累灌注不良属于Ⅱ 型的比例:腹腔干动脉15%、肠系膜上动脉9%、左肾动脉9%、右肾动脉9%; 分支血管受累灌注不良属于Ⅲ 型的比例:腹腔干动脉13%、肠系膜上动脉10%、左肾动脉0、右肾动脉28%。
32例患者均成功进行了覆膜支架腔内修复术, 无中转开胸或术中死亡病例, 手术时间平均2 h, 无术中输血病例。本组患者TEVAR术中所用均为覆膜支架, 型号包括:TAG (Gore, USA)、Zenith (Cook, USA)、Endurant (Medtronic, USA)、Grikin (有研亿金, 中国)、MicroPort (微创, 中国)、Relay (Bolton Medical, USA)等。覆膜支架为右股动脉入路29例, 左股动脉入路3例。
采用单支覆膜支架者15例(46.9%), 长度为(189.2± 16.9) mm (171~200 mm), 近端直径为(30.6± 0.9) mm (30~32 mm)。采用两段式覆膜支架者17例(53.1%), 其中近段支架的长度为(175.6± 23.8) mm (150~200 mm), 近端直径为(31.5± 1.8) mm (30~34 mm); 远段支架的长度为(127.6± 17.9) mm (120~160 mm)。
术中造影显示内漏3例, 均为Ⅰ 型内漏, 予以球囊扩张后内漏消失, 无Ⅱ 型、Ⅲ 型内漏发生。本组病例腹腔干动脉均未覆盖, 患者术后意识状态良好, 无截瘫发生, 3例伴间歇性跛行的患者下肢缺血症状改善明显。32例患者TEVAR后即刻DSA影像示主动脉腹腔四分支血管血流灌注效果尚可, 分支血管均未做腔内重建。患者术后平均住院时间(9.1± 3.9) d (4~17 d), 术后住院期间无死亡病例。
本组患者随访时间1~6个月(平均4个月), 无失访病例。术后随访CTA显示, 假腔隔绝完全, 支架无移位及相关并发症发生。复查CTA显示, 属于“ 高危” 受累的腹腔四分支灌注不良的14支分支血管中, 13支(92.9%)显示缺血改善, 1支(7.1%)由Ⅰ -b型缺血转归为Ⅰ -c型, 患者无明显腹部不适症状, 予以密切随诊观察。本组患者腹腔四分支血管术后转归情况见表2和图3。
| 表2 32例患者腹腔四分支血管手术前后“ 高危” 和非“ 高危” 分支血管改变 Table 2 Changes of four abdominal aortic branches in 32 patients between “ high-risk” and non-“ high-risk” in pre- and post-TEVAR |
分支血管灌注不良是Stanford B型主动脉夹层的严重并发症, 治疗不及时将造成诸多器官功能障碍, 如肠缺血、下肢缺血、脊髓缺血及肾功能不全等[2]。TEVAR治疗Stanford B型主动脉夹层不仅能有效防止夹层破裂, 亦能有效改善分支血管灌注不良症状[9]。
Williams等[10]于1997年将夹层引起的分支血管灌注不良分为动力型和静力型。动力型灌注不良的分支血管仍起源于真腔, 通常由于夹层内膜片阻塞了分支血管开口而灌注不良, TEVAR因隔绝了原发破口使得真腔管径增大, 分支血管血流灌注恢复效果好。静力型灌注不良是夹层累及腹腔分支血管本身, 分支血管真腔受压变窄或阻塞。因静力型受损的分支血管灌注不良情况比较复杂, 理论上主动脉真腔血流灌注改善并不能完全缓解分支动脉缺血状态[11], 必要时需行分支血管腔内重建(revascu-larization)。具体何种类型的分支血管灌注不良需要处理临床尚无明确定论, 基于Nagamine分支血管灌注不良细化分型(Ⅰ 类属动力型, Ⅱ 类属静力型, Ⅲ 类属混合型), 本研究比较了TEVAR手术前后腹腔四分支血管灌注分型的转归情况, 评价腔内治疗对分支血管灌注不良的改善效果, 并就分支血管灌注不良是否需要腔内重建给出合理化建议。
腹腔分支动脉缺血的患者更多表现为腹痛和下肢疼痛。本组32例患者, 无明显腹腔分支动脉缺血表现, 以胸痛为主要症状入院(96.9%), 伴腹部不适入院者5例(15.6%), 下肢不适入院者3例(9.4%)。股动脉搏动不佳的患者常提示下肢动脉灌注不良, 这类患者还可能伴有术前下肢缺血症状(间歇性跛行)和急性肾功能衰竭表现(本组患者无), 同时, 腹腔分支血管灌注不良的患者发生脊髓缺血的可能性较高(本组患者无)。
本组32例患者中, 属于Ⅰ 型灌注不良的在腹腔四分支血管分类中占67.2%(86/128), 四分支血管所占比例分别为:腹腔干动脉70%、肠系膜上动脉75%、左肾动脉75%、右肾动脉47%, 其中Ⅰ -a亚型在腹腔四分支血管受累中最常见(60.9%, 78/128), 说明本组病例中半数以上夹层受累腹腔四分支血管仍起源于真腔, 腹腔脏器血流灌注未明显受损, 与Nagamine等[5]报道的分支血管受累常见Ⅰ -a亚型相一致(42.2%, 54/128), 但本组患者Ⅰ -a亚型比例更高, 这可能与入组患者既有急性期也有亚急性期和慢性期有关。属于Ⅱ 型灌注不良的腹腔四分支血管中, 腹腔干动脉受累更为常见(腹腔干动脉 vs. 肠系膜上动脉 vs. 左肾动脉 vs. 右肾动脉:15% vs. 9% vs. 9% vs. 9%), 这可能与腹腔干动脉解剖位置高, 夹层内膜片向主动脉远端撕裂时首先受累有关, 其中, “ 高危” (high-risk)Ⅱ -b-2亚型多累及腹腔干动脉(腹腔干动脉 vs. 肠系膜上动脉 vs. 左肾动脉 vs. 右肾动脉:9% vs. 3% vs. 0 vs. 0)。属于Ⅲ 型灌注不良, 自开口处内膜撕裂的Ⅲ -a亚型在腹腔四分支血管中所占比例, 腹腔干动脉和肠系膜上动脉缺血受累大致相同(腹腔干动脉 vs. 肠系膜上动脉:13% vs. 10%), 这一点不同于Nagamine等[5]报道的主动脉夹层更易造成腹腔干开口处内膜撕裂(Ⅲ -a亚型中肠系膜上动脉 vs. 腹腔干动脉:3% vs. 29%)。
值得注意的是, 本组32例夹层累及肠系膜上动脉缺血分型中无一例属于“ 高危” 型血流灌注不良(Ⅰ -b、Ⅰ -c、Ⅱ -b-2和Ⅲ -c亚型), 这部分解释了本组患者收治入院时无明显的腹腔脏器缺血症状, 当然也不能除外腹腔脏器缺血的早期表现较实际出现缺血征象延迟, 因此临床对早期缺血征象的评估较为困难[12, 13]。本组32例患者中左肾动脉无一例属于Ⅲ -a亚型, 但属于Ⅲ -a亚型的右肾动脉, 自开口处内膜撕裂所占的比例在腹腔四分支血管中最大(右肾动脉 vs. 腹腔干 vs. 肠系膜上动脉 vs. 左肾动脉:28% vs. 13% vs. 10% vs. 0), 可能与夹层第一破口位置常发生于大弯侧, 假腔内血流动力造成远端内膜撕裂的切应力对主动脉远端分支血管中处于较低解剖位置的右肾动脉影响较大相关, 这将在以后的研究中重点阐述。
Nagamine分型中, Ⅰ -a、Ⅱ -a、Ⅱ -b-1和Ⅲ -a亚型血流灌注受损不明显, 而Ⅰ -b、Ⅰ -c、Ⅱ -b-2、Ⅲ -b、和Ⅲ -c型对分支灌注影响较大, 属于“ 高危” 。本组32例患者128支血管中, 14支腹腔缺血分支属于“ 高危” 受损, TEVAR术后, 13支(92.9%)显示缺血改善, 1支(7.1%)Ⅰ -b型缺血术后转归为Ⅰ -c型, 结合患者无明显缺血症状且对二次腔内治疗较抵触, 予以密切随诊观察。理论上动力型Ⅰ -b和Ⅰ -c亚型分支灌注不良在TEVAR术后转归效果好, 本组患者有8条分支动脉属于Ⅰ -b和Ⅰ -c亚型, 除1例分支血管灌注不良(左肾动脉)由Ⅰ -b型转归为Ⅰ -c型外, 其余7条分支血管的血流灌注状态均明显改善。
对于急性主动脉夹层造成分支灌注受损明显的Ⅱ -b-2亚型, 如果腹腔分支血管周围存在一个或多个再破口, 造成TEVAR术后假腔内的不完全减压(远段再破口转变为原发破口), 可导致假腔血栓化效果欠佳, 腹腔分支血流灌注改善效果不理想。本组患者中有3例腹腔干动脉和1例左肾动脉受累属于Ⅱ -b-2型缺血, TEVAR术后血流灌注均有改善, 其中2例慢性夹层患者因假腔内有效减压使得分支灌注受损的Ⅱ -b-2转归为Ⅱ -b-1型, 另1例慢性夹层转归为Ⅰ -a型, 余1例急性夹层患者腹腔动脉周围再破口撕裂缺血分型转归为Ⅲ -a型。腹腔四分支动脉中, 肠系膜上动脉TEVAR术后转归效果最佳, 其中2例Ⅰ -a型因假腔完全闭合转归为正常型, 1例Ⅱ -a和1例Ⅲ -a型转归为Ⅰ -a型。可能的原因是本组患者主动脉夹层累及肠系膜上动脉的基础条件较好, 不存在分支血流灌注不良高危亚型, 术后原发破口隔绝使得假腔压力减低, 血栓化效果好。
Nagamine等[5]认为, 对于因夹层造成的“ 高危” Ⅰ -b、Ⅰ -c、Ⅱ -b-2、Ⅲ -b和Ⅲ -c型缺血, 为确保分支血流灌注, 无论患者有无明显腹腔脏器缺血症状都需要即刻外科或腔内治疗, 其中Ⅱ -b-2型和Ⅲ -b型缺血一旦发现即需分支动脉重建。但是, Ⅱ -b-2型和Ⅲ -b型缺血并不能一概归为静力型, Shiiya等[14]认为, 如分支动脉夹层假腔内不伴有血栓时, 分支缺血仍属动力型。本组患者中, 7例属于Ⅰ -c型分支缺血, 其中4例TEVAR术后血流灌注好转为Ⅰ -a型, 3例转归为Ⅲ -a型, 因无腹腔分支缺血表现继续随诊观察; 1例急诊夹层患者左肾动脉受累属于Ⅰ -b型缺血, TEVAR术后1个月CTA显示转归为Ⅰ -c型, 结合该患者无明显不适及复查血肌酐正常, 予以继续随诊复查。此外, 本组患者中有4例属于Ⅱ -b-2型缺血, TEVAR术中未进行分支血流重建, 术后3个月复查效果尚可, 继续随诊。原则上, 夹层累及分支属于Ⅲ -c型缺血的治疗策略是在腔内治疗的同时还需要评估缺血脏器的功能, 以决定是否有必要采用术中支架开通闭塞动脉(revascularization)或行动脉转流术(bypass)以恢复缺血分支动脉的血流灌注。本组患者中腹腔四分支动脉无Ⅲ -b和Ⅲ -c型缺血。
综上, 基于Nagamine细化分型, 本研究对于夹层累及腹腔分支动脉的腔内治疗策略是:Ⅰ 型缺血:单纯行TEVAR术+随诊复查; Ⅱ 型缺血:对于Ⅱ -a和Ⅱ -b-1型, TEVAR+随诊复查, 对于Ⅱ -b-2型, 仔细评估分支动脉假腔是否血栓, 如存在血栓需要分支动脉重建, 如无血栓可以随诊观察; Ⅲ 型缺血:对于Ⅲ -a型, 单纯TEVAR+随诊复查; 对于Ⅲ -b型, TEVAR+分支动脉重建; 对于Ⅲ -c型, 评估缺血脏器功能后决定是否分支动脉重建。本研究的不足之处在于病例数少、手术前后仅用CTA评估腹腔四分支血管灌注不良亚型, 今后研究会引入术中血管内超声(intravascular ultrasound, IVUS)以更精确评估腹腔分支血管灌注分型。
总的来说, TEVAR能有效改善夹层受累腹腔分支血管灌注不良状态, 近期效果满意, 但远期效果还需进一步观察。推广Nagamine灌注不良细化分型对于治疗夹层受累腹腔分支血管灌注不良有重要意义。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|