磁性纳米粒由表面包被或者包埋在生物相容性材料中的一种或多种无机磁性材料晶体组成[1], 在近十几年对磁性纳米粒的研究中, 超顺磁性氧化铁纳米粒(superparamagnetic iron oxide nanoparticles, SPIONs)引起了人们越来越多的关注。SPIONs是指粒径小于20 nm的具有单一磁畴的SPIONs, 其可以在外磁场作用下产生同向的极大磁矩, 而在外磁场消失后快速消磁, 无磁滞现象[2]。SPIONs的磁学特性使其能在外磁场的作用下被特异性地递送到靶向部位, 常被用做药物或基因的载体用于磁靶向的药物递送和转染[3]。当外加磁场为交变电磁场时, SPIONs可以通过磁滞效应、涡流效应、畴壁共振等作用引起磁损耗, 将磁场能转化为热能, 造成局部温度的升高, 已经有许多报道将SPIONs用做肿瘤局部热疗的产热介质, 诱导肿瘤细胞的杀伤[4, 5]。此外, SPIONs在外磁场作用下可以引起局部的磁场不均匀, 加速周围水质子的自旋失相位, 缩短质子横向弛豫时间(transverse relaxation time, T2), 产生可检测的磁共振成像(magnetic resonance imaging, MRI)信号, 基于SPIONs的Feridex是临床上使用最广泛的T2类MRI造影剂[2]。制备同时具有良好的磁靶向性、发热性能和MRI性能的SPIONs, 有利于将磁靶向递送、热疗和MRI诊断结合用于肿瘤的诊疗。
SPIONs的制备方法有很多种, 包括水热法、溶剂热法、共沉淀法、热分解法、微乳化法等[2], 其中, 共沉淀法是目前最常用的方法之一。与其他方法相比, 共沉淀法制备过程更简单, 对反应条件要求低, 且制备量较大, 通过在制备过程中直接加入生物相容性良好的材料作为表面修饰剂, 即可得到分散性和生物相容性良好的SPIONs[6]。修饰材料可以是亲水性、亲油性材料或两亲性材料[5], 文献报道, 经亲水性材料修饰后, SPIONs的水溶性和胶体稳定性得到改善, 生物相容性得到提高, 在血液中的循环时间也得到延长, 满足了生物医学应用的要求。目前报道的对SPIONs进行表面修饰的亲水性材料分为小分子和聚合物, 包括月桂酸、右旋糖酐、聚乙二醇、聚乙二醇二羧酸、吡咯烷酮、聚丙烯酸、聚乙烯醇等[2]。
本研究以小分子柠檬酸钠为稳定剂, 通过共沉淀法制备柠檬酸(citric acid, CA)修饰的SPIONs(CA-SPIONs), 并系统地对CA-SPIONs的磁响应性、形态、粒径、磁学性质、X射线衍射图谱、红外特征、发热性能和弛豫效能等进行表征, 以明确其用于磁靶向、热疗和MRI等的相关理化性质, 为该纳米粒进一步应用于肿瘤的靶向诊疗奠定研究基础。
六水合三氯化铁(FeCl3· 6H2O, 分析纯)和七水合硫酸亚铁(FeSO4· 7H2O, 分析纯)购自天津市光复科技发展有限公司, 二水合柠檬酸三钠(分析纯)和氨水(质量分数为25%, 分析纯)购自北京化工厂, 工业氮气(≥ 99.5%)购自北京千禧京城气体销售中心, 实验中用水均为去离子水。
本研究所用的主要仪器有:PL203电子天平(上海梅特勒-托利多仪器有限公司)、HH-2数显恒温水浴锅(常州国华电器有限公司)、JJ-1精密增力电动搅拌器(金坛市江南仪器厂)、TGL-16M高速台式冷冻离心机(长沙湘仪离心机仪器有限公司)、FD-1D-80真空冷冻干燥机(北京博医康实验仪器有限公司)、JEM-1200EX透射电子显微镜(日本JEOL公司)、Malvern Zetasizer Nano ZS激光粒度测定仪(英国 Malvern instruments公司)、HH-15 振动样品磁强计(南京南大仪器有限公司)、MiniFlex 600 X射线衍射仪(日本Rigaku公司)、Nexus 470红外光谱仪(美国尼高力仪器公司)、Q600 SDT热重-差热同步分析仪(美国TA公司)、15 kW晶体式高频感应加热机(东莞市震森实业有限公司)、3.0 T MRI扫描仪(GE Medical Systems, 美国LLC公司)、DRC-Ⅱ 电感耦合等离子体质谱仪(ICP-MS, 美国Perkin Elmer公司)。
称取5.13 g FeCl3· 6H2O和2.78 g FeSO4· 7H2O于三口瓶中, 加入100 mL经煮沸除去氧气的去离子水, 在搅拌下使其完全溶解。将三口瓶置于60 ° C的恒温水浴, 通氮气保护, 在900 r/min的搅拌速度下加入15.5 mL的氨水, 反应30 min, 再称取2.65 g二水合柠檬酸三钠溶于20 mL去氧水中, 加入到三口瓶中, 将水浴温度升高到80 ℃, 继续搅拌反应1 h, 冷却至室温。将所得混悬液在6 000 r/min下离心15 min, 弃去上层液体再加水重悬, 继续离心洗涤至溶液呈中性, 加水重新分散下层沉淀, 即得到CA-SPIONs的水分散液, 取部分纳米粒冻干, 其余样品置于4 ℃冰箱中保存备用。
1.4.1 外观及磁响应性 取适量CA-SPIONs的水分散液置于透明西林瓶中, 观察外观并拍照, 再将一直径为1.5 cm的圆形磁铁放置在西林瓶的一侧, 观察溶液的移动情况并拍照。
1.4.2 透射电子显微镜 将CA-SPIONs的水分散液适当稀释, 滴于碳支持膜双联铜网上, 室温下自然晾干, 采用透射电子显微镜(transmission electron microscope, TEM)在加速电压为120 kV的条件下对纳米粒进行形态和粒径表征。
1.4.3 水力学粒径 取少量CA-SPIONs的水分散液适当稀释后, 采用激光粒度仪通过动态光散射(dynamic lighting scattering, DLS)对CA-SPIONs的水力学粒径及其分布情况进行测定, 平行测定3次。
1.4.4 红外光谱 将适量冻干的CA-SPIONs与溴化钾(potassium bromide, KBr)粉末混合均匀后, 用压片机压成圆盘状薄片, 采用傅里叶转换红外(Fourier transform infrared spectroscopy, FT-IR)光谱仪在4 000~400 cm-1的范围内进行测定。
1.4.5 热重分析 采用热重-差热同步分析仪对CA-SPIONs进行热重分析(thermogravimetric analysis, TGA), 氮气氛围下进行测定, 升温范围为室温至800 ℃, 升温速度为10 ℃/min。
1.4.6 磁学性质 采用振动样品磁强计在室温下对CA-SPIONs的磁化曲线进行测定, 外加磁场范围为± 6 kOe, 并根据所得曲线计算CA-SPIONs的饱和磁化强度、剩余磁化强度和矫顽力等磁学性质参数。
1.4.7 X射线衍射图谱 采用X射线衍射仪(Cu靶, Kα 线, λ =0.154 186 7 A), 在40 kV、15 mA下测定CA-SPIONs的X射线衍射(X-ray diffraction, XRD)图谱, 对超顺磁性氧化铁(superparamagnetic iron oxide, SPIO)的物相进行分析。扫描范围为10° ~80° , 步长0.02° , 扫描速度为5° /min。
取CA-SPIONs的水分散液, 加水稀释至SPIO的浓度为10 g/L。取1 mL稀释后的样品溶液置于2 mL Ep管中, 将Ep管固定在高频感应加热机环状铜线圈的中心后开机, 调节加热电流为9 A并开始计时, 此时仪器的工作频率在45~50 kHz的范围内, 通过温度计测定15 min内样品溶液的温度变化, 平行测定3次。
比吸收率(specific absorption rate, SAR)的计算[7]:根据测得的数据绘制温度随时间变化的曲线, 代入公式SAR=(C× Δ T/Δ t)/mFe进行计算, 其中C为样品特异性的加热能力(J/K), 是Fe3O4和水的质量加权平均数, 对于Fe3O4,
将CA-SPIONs的水分散液配制成铁离子浓度(0.9、1.8、3.5、7.0和14.0 mg/L)逐渐增加的5个样品溶液, 将配好的溶液转移至Ep管中, 置于3.0 T的MRI扫描仪下, 采用头线圈进行T2加权成像扫描, 扫描序列为快速自旋回波序列, 脉冲重复间隔时间为3 000 ms, 回波时间105 ms, 断层厚度5.0 mm, 视野240 mm× 240 mm, 翻转角111° , 矩阵256× 256, 信号激励次数为2。
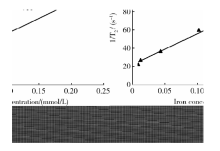
横向弛豫效能(transverse relaxivity, r2)的测定:保持Ep管的位置不变, 继续采用头线圈对不同浓度样品溶液进行T2 MAP图像扫描, 扫描参数如下:采用自旋回波系列, 固定脉冲重复间隔时间为800 ms, 回波时间分别为5.74、11.48、17.22、22.96、28.7、34.44、40.18和45.92 ms, 断层厚度5.0 mm, 视野200 mm× 200 mm, 翻转角90° , 矩阵256× 256, 信号激励次数为2, 共获得8个回波图像, 采用感兴趣区(region of interest, ROI)程序分别测定T2 MAP图像不同浓度样品溶液的T2值, 并通过ICP-MS对各个样品溶液的铁离子浓度进行精确的测定。根据公式:1/T2=1/T2, 0+r2C, 其中T2为观察到的横向弛豫时间(s), T2, 0为加入造影剂前的横向弛豫时间(s), r2为横向弛豫效能[(mmol/L)-1· s-1], C为铁离子的浓度(mmol/L), 做1/T2随铁离子浓度变化的曲线, 并进行线性拟合, 所得曲线的斜率即为CA-SPIONs的
2.1.1 外观及磁响应性 如图1所示, CA-SPIONs的水分散液呈深黑色, 分散均匀, 在磁铁的作用下被快速吸引到西林瓶的一侧, 磁响应性良好, 当外部磁铁位置发生变化时, 磁流体也可以随之移动。
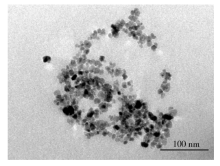
2.1.2 TEM 图2为CA-SPIONs的透射电镜照片, 从图中可以看出经CA修饰后的SPIONs为黑色球形, 大小均匀, 分散性良好, 无团聚, 平均粒径在12 nm左右。
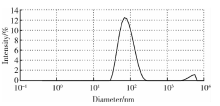
2.1.3 水力学粒径 图3为CA-SPIONs的水力学粒径分布图, 经3次测定其平均粒径为(72.35± 4.47) nm, 多分散系数为0.231 ± 0.029, 表明CA-SPIONs在水中分散均匀, 没有出现明显的团聚。与TEM结果相比, CA-SPIONs水力学粒径的增大与纳米粒表面的有机物修饰有关[9]。
2.1.4 红外光谱 图4A、B分别为二水合柠檬酸三钠和CA-SPIONs的FT-IR图谱。在图4A中, 3 454 cm-1处出现的为— OH的伸缩振动峰, 2 800 cm-1到3 000 cm-1间的谱带代表— CH2的伸缩振动峰, 1 590 cm-1和1 394 cm-1处的吸收峰分别为COO-基团不对称伸缩振动峰υ as(COO-)和对称伸缩振动峰υ s(COO-)。在图4B中, 3 422 cm-1处出现的为— OH的伸缩振动峰, 可能来自于SPIONs表面的羟基, 也可能来自于SPIONs表面修饰的柠檬酸钠的羟基。在1 619 cm-1和1 399 cm-1处的吸收峰分别为COO-基团不对称伸缩振动峰υ as(COO-)和对称伸缩振动峰υ s(COO-), 与二水合柠檬酸三钠COO-的特征吸收峰相对应。此外, 在588 cm-1处出现的为Fe— O键的伸缩振动峰, 红外结果证明SPIONs表面成功修饰上了CA[10]。
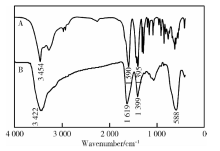 | 图4 二水合柠檬酸三钠(A)和CA-SPIONs(B)的红外光谱图Figure 4 FT-IR spectra of trisodium citrate dehydrate (A) and CA-SPIONs (B) |
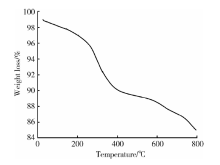
2.1.5 TGA 图5为CA-SPIONs的TGA曲线, 其中低于180 ℃的重量损失可能是由于样品中残余水分、样品表面吸附的水分蒸发及纳米粒表面CA失去结晶水而产生的, 此后样品表面不再含有水分, 在室温至180 ℃的温度范围内样品失重 2.6%, 即样品中水分所占质量分数为 2.6%。在180~600 ℃范围内的重量损失则是由于纳米粒表面修饰的CA分解所造成的, 在此温度范围内样品失重为 9.0%, 即证明样品中CA所占质量分数大约为 9.0%。600~800 ℃之间的失重为Fe— O— C键的断裂及分解所造成的, 800 ℃时样品残留重量为85.0%, 即CA-SPIONs中残留的SPIO所占的质量分数大约为85.0%[11]。
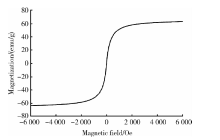
2.1.6 磁学性质 图6为CA-SPIONs在室温下测得的磁化曲线, 从图中可知CA-SPIONs的饱和磁化强度为63.58 emu/g, 剩余磁化强度为0 emu/g, 矫顽力为636.94 A/m, 在磁化曲线中无磁滞环出现, 证明CA-SPIONs具有良好的超顺磁性, 其磁学性质未受到CA包被的影响。
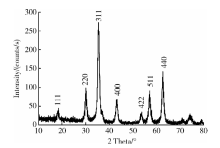
2.1.7 XRD CA-SPIONs的XRD图谱如图7所示, 图中CA-SPIONs在18.1° 、30.1° 、35.5° 、43.3° 、53.6° 、57.1° 和62.9° 处的衍射峰分别与Fe3O4(111)、(220)、(311)、(400)、(422)、(511)和(440)的晶相(JCPDS No. 85-1436)相对应, 证明CA-SPIONs为反尖晶石结构[12]。此外, CA-SPIONs的各个窄而高衍射峰均表明SPIO的结晶度高, 具有良好的晶型。由Debye-Scherrer半宽公式[13]:D=kλ /(β cosθ ), 其中k为Scherrer常数(0.95), D为晶粒粒径, λ 为测试波长, β 为衍射峰半高宽, θ 为衍射角, 和CA-SPIONs在(311)晶相处的衍射峰可以计算出SPIO的平均晶粒大小为12.4 nm, 与TEM观察到的结果相一致。
图8为含10 g/L SPIO时, CA-SPIONs在电流为9 A, 45~50 kHz的交变电磁场作用下的升温曲线, 在15 min内CA-SPIONs水分散液的温度从21.8 ℃升高到了47.5 ℃, 经计算其SAR值为26 W/g。
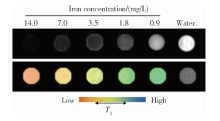
不同铁离子浓度的CA-SPIONs水分散液测定的T2加权MRI图像和T2 MAP图像如图9所示, 以测定的T2值的倒数对铁离子浓度做线性回归, 所得拟合曲线如图10所示, 其方程为y=338x+22.2, R2=0.994, 则CA-SPIONs的r2为338 (mmol/L)-1· s-1, 高于市售的T2类造影剂Feridex的r2[260 (mmol/L)-1· s-1][14], 说明CA-SPIONs有希望用于MRI检测。
磁靶向是指利用外加高梯度磁场, 将装载了药物或基因的磁性纳米粒通过血液循环递送到体内特定位点, 达到增加药物摄取或基因转染效率的同时避免引起系统性损伤的目的[3]。良好的磁响应性是SPIONs用于磁靶向的前提, 磁响应性实验证实, CA-SPIONs在外磁场作用下能快速响应, 能随外磁场的变化而相应移动, 满足用于磁靶向的基本要求。此外, 大的比表面积和良好的稳定性也是SPIONs用于在体磁靶向递送的基本要求, 通过在共沉淀过程中加入柠檬酸钠, 柠檬酸钠电负性的羧基可以与溶液中大量微小纳米晶核上缺电子的铁原子配位, 形成共轭结构而结合到粒子表面, 增大晶核间的静电斥力和空间位阻, 阻止晶核的聚集和长大, 从而制备出粒径较小、比表面积大的SPIONs[15]。经TEM观察可知, CA-SPIONs粒径均小于20 nm, 且均匀分散, 与预期实验结果一致。此外, 经柠檬酸修饰后, CA-SPIONs呈现出了良好的水分散性和胶体稳定性, 其柠檬酸的包被层也可以保护SPIO的内核不被空气中的氧气所氧化。CA-SPIONs水力学粒径明显大于TEM结果, 是因为在TEM下只能观察到纳米粒晶核的大小而观察不到纳米粒表面的有机物包被层, 而DLS测定的是纳米粒水化层的厚度。如文献中报道的右旋糖酐修饰的SPIONs在TEM下的粒径为10 nm, 而水力学粒径为168.6 nm[14], 文献中报道的聚乙二醇修饰的SPIONs在TEM下粒径为8 nm, 而水力学粒径在70~140 nm的范围内[16]。经验证, CA-SPIONs的水分散液在4 ℃下保存1个月仍为黑色均匀的溶液, 无纳米粒的沉淀生成。
本研究中CA-SPIONs的饱和磁化强度为63.58 emu/g, 根据热重分析结果(SPIO的质量分数为85%)归一化处理后, 纯的SPIO的饱和磁化强度可以达到74.8 emu/g, 高的饱和磁化强度可以使得纳米粒能对外加磁场快速响应。此外, SPIONs的饱和磁化强度也与其MRI对比增强作用直接相关, 饱和磁化强度越大, 其相应的横向弛豫率R2(T2的倒数)就越大, 即引起水质子T2缩短的效应越强, T2加权MRI下对比增强效果越显著[17]。XRD结果表明, 当Fe3+ :Fe2+的摩尔比为1.9 :1时, 也可以生成反尖晶石相的Fe3O4, 这可能是因为实验过程中会有少量O2混入, 导致部分Fe2+被氧化成Fe3+。即使有部分γ -Fe2O3生成或者部分Fe3O4被氧化成了γ -Fe2O3, 生成的γ -Fe2O3也同样具备用于磁靶向、热疗和MRI的特性[8, 17]。
由于肿瘤细胞处于乏氧、低pH的环境中, 细胞代谢旺盛, 但组织结构和细胞器发育不完全, 而且肿瘤组织内部的血液循环受到阻碍导致散热能力有限, 因此肿瘤细胞与正常组织相比对热更加敏感。此外, 热疗过程中的高热(41~46 ℃)会激活机体的免疫应答, 对肿瘤细胞形成非特异的杀伤而避免了对正常组织的影响[18]。根据CA-SPIONs的温度-时间曲线可知, 在9 A和45~50 kHz的交变电磁场作用下, CA-SPIONs被加热到41 ℃仅需9 min, 升温过程快速、高效。SAR值反映了单位时间内单位质量的磁性纳米粒将磁能转化为热能的比率, SAR值越高说明磁性纳米粒的产热效应越好, 达到相同温度所需纳米粒的用量和时间就越少, 其值的高低主要依赖于交变电磁场的强度(电流和振幅)、纳米粒子本身的性质和测定时的浓度[18]。在已报道的文献中, 由于交变电磁场条件、SPIONs修饰材料和制备方法以及实验时所用浓度的不同, 测得的SAR值差异很大。如商品化的FluidMag-HS在10 g/L Fe浓度和290 kHz、12 kA/m的交变电磁场下, 测得的SAR值仅为19 W/g[7], 而多种方法制备的右旋糖酐修饰的SPIONs在3 mg Fe3O4/mL的浓度和292 kHz、58 kA/m的交变电磁场下测得的SAR值最大可以达到384 W/g[19], 此外, Kulshrestha等[20]制备的CA-SPIONs在423 kHz、10 kA/m的磁场下测定的SAR值也仅为21.5 W/g。与文献中报道的实验条件相比, 本研究所采用的交变电磁场条件相对较低, 虽然CA-SPIONs测得的SAR值只有26 W/g, 但当外加电磁场条件进一步增强时, 其SAR值仍有望进一步升高, 发挥出更强的热疗作用。此外, 就纳米粒本身的性质来说, SAR值的高低大体上与纳米粒本身的饱和磁化强度和磁晶各向异性常数成正比, 与纳米粒的粒子分布成反比, 我们所制备的CA-SPIONs的高饱和磁化强度和单分散性均使其有希望成功用于肿瘤的热疗。
与临床中其他成像模式相比, MRI具有空间分辨率高、软组织对比度高、解剖学细节清晰的优点, 在临床诊断中发挥着重要作用, 据统计有30%的临床MRI检查需要使用对比剂来进一步改变水质子的弛豫时间以形成足够强的检测信号[11]。从CA-SPIONs的T2加权图像上可以看出, CA-SPIONs呈现出良好的负性对比增强作用, 可以产生明显的低信号区域, 且信号强度随着铁离子浓度的增加而逐渐降低, 当铁离子浓度低至0.09 mg/L时仍可以产生明显的低于水的暗信号。r2代表了造影剂的横向弛豫效能, 当r2越大时, 其引起水质子的T2缩短就越多, 产生的磁共振对比就越显著。本研究制备的CA-SPIONs的r2为338 (mmol/L)-1· s-1, 高于市售的Feridex [260 (mmol/L)-1· s-1], 证明我们所制备的CA-SPIONs能够满足临床上对T2类造影剂弛豫效能的要求, 有希望用于肿瘤的MRI检测。
综上所述, CA-SPIONs具有良好的磁响应性和高饱和磁化强度, 在交变电磁场下具有良好的发热性能, 在MRI扫描下具有优异的弛豫效能和显影效果, 有希望用于磁靶向、热疗和MRI诊断。
(志谢:感谢中国人民解放军总医院临床药理研究室的刘屏老师在交变电磁场加热设备上所提供的帮助。)
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|