1 资料与方法
1.1 患者资料
1.2 机器人辅助腹腔镜移植肾切除手术步骤
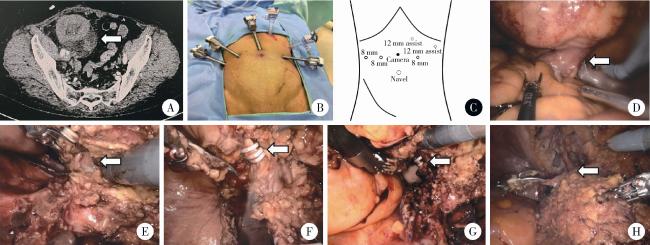
图1 机器人辅助腹腔镜移植肾切除术(右侧为例)术前影像、穿刺孔布局及关键手术步骤图Figure 1 Preoperative imaging, trocar placement, and key surgical steps of robot-assisted laparoscopic transplant nephrectomy (right side as an example) A, preoperative imaging with the arrow indicating the transplanted kidney in right pelvic; B, C, example of trocar placement; D, the transplanted kidney was suspended in the extraperitoneal space, with the arrow indicating the anastomosis site between the renal pedicle and the iliac vessels; E, the arrow showed that the transplanted renal artery sheath was significantly thickened; F, the arrow showed that the transplanted renal artery was dissected and occluded with Hemolock clips, the blue vascular suture was visible at the anastomotic site; G, the arrow showed that the transplanted renal vein was dissected and occluded with Hemolock clips; H, the arrow showed that the ureter of transplanted kidney was dissected and occluded with Hemolock clips. |
2 结果
表1 机器人辅助腹腔镜移植肾切除患者的基本信息Table 1 Basic information of patients undergoing robot-assisted laparoscopic transplant nephrectomy |
| Characteristics | Case 1 | Case 2 | Case 3 | Case 4 | Case 5 |
| Gender | Male | Female | Female | Female | Male |
| Age/years | 33 | 68 | 60 | 31 | 37 |
| Body mass index/(kg/m2) | 17.83 | 24.24 | 20.73 | 14.57 | 21.05 |
| Duration since kidney transplant/years | 3 | 18 | 22 | 10 | 6 |
| Number of transplanted kidneys | 1 | 1 | 1 | 1 | Double kidney transplant, removal of the left transplanted kidney |
| Indications for transplant nephrectomy | Recurrent hematuria and fever | Recurrent hematuria | Recurrent hematuria and abdominal pain | Mass of transplant kidney | Hydronephrosis with recurrent pyelonephritis |
| Operative time/min | 351 | 220 | 212 | 150 | 145 |
| Blood loss/mL | 300 | 500 | 150 | 300 | 20 |
| Postoperative stay of hospital/d | 7 | 6 | 8 | 25 | 4 |
| Perioperative complications | Injury of the external iliac artery | None | None | Cardiac failure and infection | None |
| Conversion to open surgery | No | No | No | Yes | No |
| Perioperative motality | No | No | No | No | No |
| Pathological results | End-stage nonfunctioning kidney | End-stage nonfunctioning kidney | End-stage nonfunctioning kidney | BK virus-associated urothelial carcinoma | Chronic pyelonephritis with renal parenchymal atrophy |