下颌骨位于颌面部中下1/3,通过双侧颞下颌关节与颅面部其他骨骼连接,是颌面部最大的骨骼,也是唯一可以活动的骨骼[1]。下颌骨对维持面下1/3形态,保持口腔咀嚼、吞咽、言语等功能起着重要作用,是口腔颌面部最重要的功能器官之一[2-3]。随着CT技术的普及和数字诊断分析技术的发展,下颌骨三维形态分析已成为口腔临床疾病诊断、治疗设计和疗效评价的重要环节,下颌骨解剖标志点是体现下颌骨三维形态的重要解剖特征,标志点的准确确定是下颌骨三维形态分析的前提和基础。既往研究显示,三维下颌骨标志点可用于构建下颌骨正中矢状平面,对下颌骨的对称性进行量化评价[4];可用于预测下颌骨缺损区域的正常颌骨形态,为下颌骨的重建治疗提供参考[5-6];可用于辅助分析正颌或肿瘤患者面部软硬组织变化规律,利于医患沟通[7];由下颌骨标志点衍生的多种形态学测量指标,也可用于评价青少年下颌骨三维空间发育趋势[8]。上述研究中,下颌骨标志点的确定主要以人工标记为主,人工定点工作量大、经验依赖性强,不利于临床普及推广。目前在颅颌面CT断层扫描片上进行自动化确定颅骨标志点的研究相对较多,主要包括基于知识类[9]和基于机器学习类[10-12]两类方法,而在三维下颌骨数据上自动确定标志点的相关研究仍然较少。
为实现快速、准确、自动、灵活地确定下颌骨三维数字模型解剖标志点的临床需求,本研究尝试探索一种基于三维下颌骨平均模型非刚性变形的标志点自动确定方法,通过构建1例一定程度上体现我国青年人群下颌骨形态特点的三维下颌骨结构化平均模型(即“下颌骨模板”),结合非刚性配准算法实现下颌骨模板数据与患者个体化下颌骨数据的变形匹配[13],从而实现下颌骨模板标志点到患者下颌骨数据的映射转移,实现解剖标志点的快速、自动确定。
1 资料与方法
1.1 研究对象
选取就诊于北京大学口腔医院的40例颅颌面三维形态正常患者的CT数据(其中30例用来建立三维下颌骨平均模型,10例作为测试本研究方法确定下颌骨标志点效果的测试数据),患者16~45岁,男女比例约为1:1。本研究获得北京大学口腔医院生物医学伦理委员会批准(PKUSSIRB-202164079),受试者均对本研究内容和目的充分知情并签署知情同意书。
纳入标准:(1)CT数据完整,扫描范围覆盖颌面部中下2/3;(2)下颌骨完整,无CT上可见的骨缺损、破坏、吸收;(3)牙齿排列基本整齐、前牙覆
排除标准:(1)颞下颌关节紊乱病的患者;(2)有正畸治疗史、正颌治疗史、下颌骨外伤史及下颌骨手术史的患者;(3)存在严重错
1.2 实验设备及软件
临床数据获取使用的CT设备为i-CAT(Imaging Sciences International,美国);数据处理和分析软件使用三维影像学软件Mimics 24.0(Materialise,比利时)、三维逆向工程软件Geomagic Wrap 2021(3D System,美国)、科学计算软件MATLAB R2019b(MathWorks,美国)、开源非刚性配准程序Meshmonk(比利时)、三维几何网格处理软件MeshLab 2020(意大利)。
1.3 三维下颌骨结构化平均模型的建立流程
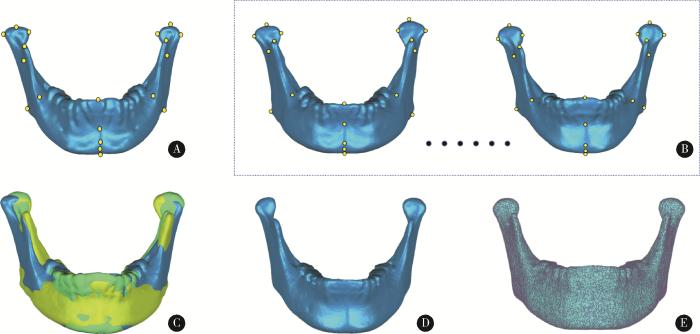
三维下颌骨结构化平均模型(即“下颌骨模板”)的构建是实现下颌骨标志点自动确定的关键环节,其建立方法的流程如图 1所示。
图1
图1
三维下颌骨模板的构建流程
Figure 1
Construction process of three-dimensional mandibular template
A, alignment reference data for size-normalization and alignment of 3D mandible data, showing 19 markers (yellow) required for the Procrustes analysis algorithm; B, 3D mandibular data of the remaining 29 patients except the alignment reference data; C, results after size-normalization and alignment of patients' 3D mandibular data; D, 3D average model of mandible based on 3D mandibular data of 30 patients; E, 3D mandibular structured template based on 3D mandibular average model.
1.4 三维下颌骨数据的尺寸归一化与对齐
将40例患者的CT数据分别导入Mimics 24.0软件,通过选择合适的阈值(450~800 HU)创建下颌骨蒙版,辅助人工对蒙版的精细化调整,三维重建每个患者的下颌骨三维模型,输出.STL格式数据。将下颌骨.STL数据导入Geomagic Wrap 2021软件中,删除三维模型内部的三角面片数据,再通过平滑、填充孔等数据修复功能对下颌骨模型的缺陷进行处理,通过增强网格功能创建出三角面片数量约为4万的下颌骨模型。使用Geomagic软件的“点特征”功能,由同一名口腔医师对上述每例患者三维下颌骨数据标记19个解剖标志点,其中包括14个双侧标志点(右髁突顶点、左髁突顶点、右髁突最外侧点、左髁突最外侧点、右髁突最内侧点、左髁突最内侧点、右喙突顶点、左喙突顶点、右乙状切迹最低点、左乙状切迹最低点、右下颌角点、左下颌角点、右下颌升支前缘点、左下颌升支前缘点,序号分别为1~14)和5个中线标志点(颏前点、颏下点、颏顶点、下切牙点、下齿槽座点,序号分别为15~19),具体见表 1。每个标志点重复定点3次,记录标志点坐标值。对操作者3次选取标志点的可重复性进行评价,计算各标志点X、Y、Z坐标值的组内相关系数(intraclass correlation coefficient,ICC)值均为0.99~1.00,提示操作者3次选点的一致性较好,计算3次坐标值的均值作为下颌骨模型标志点专家定点的最终结果。
表1 模板法确定三维下颌骨标志点的定点误差
Table 1
| Number | Name of landmarks | Abbreviations | Distance error/mm, $\bar x \pm s$ |
| 1 | Condylion (right) | CoR | 1.94±0.60 |
| 2 | Condylion (left) | CoL | 2.24±0.97 |
| 3 | Condyle lateral point (right) | CLPR | 0.77±0.50 |
| 4 | Condyle lateral point (left) | CLPL | 0.96±0.38 |
| 5 | Condyle medial point (right) | CMPR | 1.43±0.53 |
| 6 | Condyle medial point (left) | CMPL | 1.37±0.44 |
| 7 | Coronoid process (right) | CPR | 1.01±0.44 |
| 8 | Coronoid process (left) | CPL | 0.56±0.14 |
| 9 | Lowest point of the sigmoid notch (right) | LPSNR | 1.00±0.60 |
| 10 | Lowest point of the sigmoid notch (left) | LPSNL | 0.75±0.37 |
| 11 | Gonion (right) | GoR | 2.23±0.73 |
| 12 | Gonion (left) | GoL | 1.82±1.17 |
| 13 | Lowest anterior ramus (right) | LARR | 2.52±0.95 |
| 14 | Lowest anterior ramus (left) | LARL | 2.57±1.10 |
| 15 | Pogonion | Pog | 0.83±0.36 |
| 16 | Menton | Me | 1.04±0.39 |
| 17 | Gnathion | Gn | 0.84±0.32 |
| 18 | Lower incisor | LI | 0.72±0.39 |
| 19 | Supramental | B | 2.33±1.06 |
根据中国汉族成年人群下颌骨三维测量数据库的尺寸数据[14],成年人下颌升支宽度在下颌切迹水平的平均值约为39.74 mm,下颌升支全高度的平均值约为63.78 mm,下颌角间宽度平均值约为102.47 mm,下颌髁突间宽度约为122.28 mm,下颌角角度平均值约为123.11°。从本研究构建的40例患者三维下颌骨数据中,选择与文献报道下颌骨各特征均值最为接近的1例下颌骨数据作为“对齐基准数据”,该例患者的数据为:下颌升支宽度在下颌切迹水平为42.28 mm,下颌升支全高度为63.53 mm,下颌角间宽度为105.33 mm,下颌髁突间宽度为122.74 mm,下颌角角度为121.69°。调整“对齐基准数据”至自然头位状态。
在其余39例下颌骨数据中,选择各特征值较为接近文献报道特征值的29例下颌骨数据(个体下颌骨数据),与“对齐基准数据”共同作为计算下颌骨平均模型的原始数据(合计30例)。将29例个体下颌骨数据与1例“对齐基准数据”的19个标志点坐标集文件(.csv格式)导入MATLAB R2019b软件,使用软件的普氏分析(Procrustes analysis,PA)算法函数[15]分别计算29例个体下颌骨数据相对“对齐基准数据”的尺寸缩放系数和旋转矩阵。MATLAB R2019b中的PA算法可对具有一一对应关系的点集进行最优匹配重叠,本研究使用该算法可实现对29例个体下颌骨标志点集与“对齐基准数据”标志点集的最优匹配,进而获得将29例个体下颌骨数据向“对齐基准数据”进行尺寸归一和匹配对齐的变换参数(尺寸缩放系数、坐标变换矩阵),最终获得如图 1C所示的30例三维下颌骨数据的重叠效果。
1.5 三维下颌骨平均模型的结构化处理
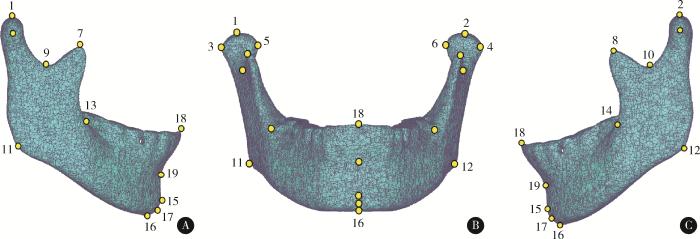
在Geomagic软件中使用计算“平均模型”的功能,计算上述尺寸归一和重叠对齐后30例三维下颌骨数据的平均形状模型,获得1例三维下颌骨平均模型。为构建配合非刚性配准算法的“三维下颌骨模板”,需对三维下颌骨平均模型进行结构化处理:(1)在Geomagic软件中对三维下颌骨平均模型使用“移动到原点”功能将模型几何中心与坐标原点重合;(2)使用“特征平面”功能构建三维下颌骨平均模型的正中矢状平面,并删除半侧下颌骨数据;(3)基于正中矢状平面使用镜像功能,创建镜像侧下颌骨数据,联合左右侧下颌骨点云数据,曲率采样并重复进行三角网格剖分,获得点数为19 915的三维下颌骨模板;(4)使用Meshlab 2020软件中的“Get Info”功能(可选取点云数据的定点并显示其序号和坐标),确定并记录三维下颌骨模型上常用的19个标志点信息(图 2、表 1)。
图2
图2
三维下颌骨模板及19个解剖标志点
Figure 2
3D mandibular template and 19 anatomical landmarks
1.6 基于“模板法”自动确定下颌骨解剖标志点
以1.4小节中计算的19个下颌骨解剖标志点3次重复确定的坐标平均值作为参考值。应用本研究构建的三维下颌骨模板结合非刚性配准算法,采用模板法确定10例患者三维下颌骨数据的19个解剖标志点坐标,计算模板法所确定的每个标志点坐标与参考值的误差,并计算所有标志点的平均误差,评价模板法确定三维下颌骨解剖标志点的定点效果。
2 结果
图3
图3
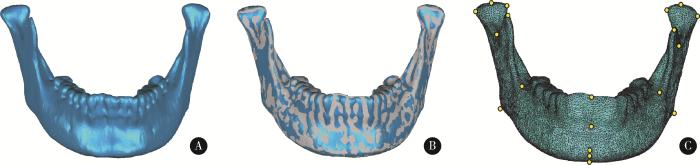
模板法确定下颌骨解剖标志点的效果
Figure 3
The result of determining mandibular anatomical landmarks by template-method
A, 3D mandible of a tested patient; B, 3D mandible template (grey) deformated and mapped to the tested 3D mandible data (blue); C, locations (yellow) of anatomical landmarks determined on the deformated 3D mandibular template.
受测试的10例患者三维下颌骨数据均可成功定位19个标志点。10例三维下颌骨数据与模板变形后数据的平均三维偏差为(0.22±0.09) mm。19个标志点的平均定点误差为(1.42±0.95) mm,其中喙突顶点的定点误差最小,左侧为(0.56±0.14) mm,右侧为(1.01±0.44) mm;下颌升支前缘点的定点误差最大,左侧为(2.57±1.10) mm,右侧为(2.52±0.95) mm。5个中线标志点中,下齿槽座点定点误差最大,为(2.33±1.06) mm,其余4个点定点误差均≤1 mm,中线标志点的平均定点误差为(1.15±0.60) mm。14个双侧标志点中,除下颌角点、髁突顶点、下颌升支前缘点外,其余各点的定点误差均小于1.5 mm,双侧标志点的平均定点误差为(1.51±0.67) mm。模板法对本研究的10例测试数据中线标志点的定点效果优于双侧标志点。
3 讨论
3.1 三维颅颌面标志点的自动确定是口腔临床诊疗发展的趋势
随着医疗数字化水平的不断提升与医学影像硬件的进一步普及,目前口腔临床颅颌面疾病的诊断分析手段已由二维照片、X线片头影测量分析逐渐发展到锥形束CT、螺旋CT、MRI等三维体层数据的测量分析,再到三维点云格式的颅颌面数据测量分析。三维数据能够更好地反映患者口腔颌面部的真实三维特征,三维标志点的确定是开展三维数据诊疗分析的基础和前提。目前在二维颅颌面影像上自动确定标志点的技术已相对成熟[17-18],而在三维颅颌面数据上确定标志点仍主要依赖手工方式,定点效率低、人力成本高,自动确定三维颅颌面数据标志点是口腔临床迫切需要解决的问题。近年来,为实现三维颅颌面标志点高效自动定位,基于软件算法自动确定标志点成为口腔临床关注的热点,目前在三维颅颌面数据上自动确定标志点的算法研究主要分为几何信息分析类算法和机器学习类算法[19]。
典型的几何信息分析类算法研究包括:2017年Liang等[20]提出了一种几何特征算法,可在三维颜面数据上自动确定鼻尖、眼眦、口角等17个标志点,对颜面几何形态变化显著区域(如鼻尖、鼻底、口角等)标志点的定点效果较好,对几何变化不显著区域的标志点定位效果不理想,算法确定标志点的数量有限;2018年Neelapu等[9]设计了一种基于颅骨对称性特征的标志点自动检测算法,将正中矢状面分为4个象限,在解剖轮廓上自动检测出标志点,20个标志点的总平均误差为1.88 mm。机器学习类算法近年来备受关注:2018年Wang等[21]和2019年Paulsen等[22]基于卷积神经网络,通过机器学习的方式在三维颜面数据上自动确定标志点,可分别确定73个和68个标志点,使用三维人脸数据库进行测试,部分标志点的定位误差分别为(2.42±0.36) mm和(3.96±2.55) mm;2019年Zhang等[10]采用2个U-net结构的上下文引导的全卷积神经网络(fully conventional networks)行关节骨分割和标志点数字化,并提出一种联合骨分割和标志点数字化的深度学习框架[11],获得了更精确的分割结果,15个标志点的平均误差为1.10 mm。机器学习类算法的特点是数据训练过程是对训练集数据特征信息的深度挖掘,针对带有人工标记的一定数量标志点信息的训练集数据,其训练结果的智能算法也仅可输出与训练集相同的标志点信息。口腔临床各学科、不同病种诊断分析所需颌骨标志点的数量和位置不尽相同,由单一病种、形态类型和标志点数量的训练集数据训练出的智能算法不能灵活适应不同的临床需求,体现为标志点数量不可调整、未参与标注训练的标志点不能确定、不同下颌骨形态类型的算法定点效果欠佳等问题。
本研究基于构建的三维下颌骨模板和开源非刚性配准程序MeshMonk,提出基于下颌骨模板弹性变形的方法,实现了下颌骨标志点的自动定点。模板法与几何信息分析类算法相比优点在于:(1)非刚性配准算法的变形适应能力较好,其变形效果受下颌骨几何特征限制较少,因而可以确定的标志点数量足够多;(2)算法的鲁棒性较好,确定标志点的平均定点误差较小。模板法与人工智能类算法相比优点在于:(1)数据准备仅需满足下颌骨模板的建立所需,不需进行大量三维下颌骨数据的特征标注和训练;(2)算法针对下颌骨形态的计算效率较高,单例数据变形匹配时间不超过5 min。
本研究下颌骨模板法定点的局限性:(1)由于非刚性配准算法对三维模型上某一数据点的变形调整程度,受与该点相关的所有周围点位置和变形程度的共同影响,每个数据点位置的弹性变化范围具有一定的局限性;(2)三维下颌骨模板的构建基于无显著颅颌面畸形正常成年人的三维下颌骨数据,模板针对下颌骨复杂畸形数据的变形适应性仍然有限,此类下颌骨数据的标志点定点效果有待进一步改进和完善。后续研究将针对口腔临床各学科疾病类型特点、患者年龄、性别等因素构建不同分类的三维下颌骨模板,以提高非刚性配准算法的变形适合性,满足口腔临床诊疗的不同需求。
3.2 基于普氏分析归一化算法构建三维下颌骨平均模型,真实体现下颌骨形态学的关键特征
基于一定数量的三维下颌骨数据计算下颌骨平均模型,可代表特定人群下颌骨的三维形貌特征,用于人体形态学的相关研究与分析。建立有代表性的下颌骨平均模型的核心环节在于实现不同患者三维下颌骨数据之间的空间最优重叠。回顾以往构建平均解剖模型的研究,李婧宇[23]使用Geomagic Studio软件的“最佳拟合”功能,将未进行尺寸调整的187例北方汉族女性的三维颜面数据按年龄段分别重叠,基于对点云数据点坐标求均值的方法构建北方汉族女性的平均人脸模型,对面部形态衰老进行研究。Kuijpers等[24]使用迭代最近点(iterative closet point, ICP)算法,将未进行尺寸调整的60例唇腭裂患儿以及203例正常幼儿的三维颜面数据按年龄段和性别分别重叠构建平均人脸模型,分析单侧唇腭裂患儿的鼻唇沟形态。上述研究在构建平均解剖模型时,均未进行三维数据的尺寸归一处理,但客观世界同类型患者数据的整体尺寸及比例存在一定差别,对原始三维数据直接进行重叠可导致局部特征的匹配效果欠佳,从而影响平均模型的构建效果。
普氏分析算法[15]是一种应用于几何形状重叠的算法,其原理是基于同类型三维模型上具有一一对应关系的关键标志点,对模型进行空间位置变换和整体尺寸的缩放变形,以达到使三维模型上关键标志点尽可能一致的重叠效果。本研究通过普氏分析算法构建30例患者下颌骨平均模型,采用基于患者下颌骨三维数据上的19个重要解剖标志点,在进行整体尺寸归一化处理后,保证同名解剖标志点的一一对应关系,实现不同患者下颌骨三维数据标志点集间平均距离最小的重叠,从而获得30例患者下颌骨三维数据的最优重叠。普氏分析算法对解剖标志点的关注较符合口腔临床的诊断经验和习惯,并被证实具有较好的可靠性[25]。本研究普氏分析重叠算法的特点是:(1)选取了覆盖下颌骨全范围的口腔临床医师关注的19个标志点,可体现个性化下颌骨数据的整体几何特征;(2)基于三维下颌骨数据上的关键标志点,对同类型但不同大小的模型进行尺寸归一化,尺寸缩放效果不影响模型自身的解剖特征关系呈现,并有利于下颌骨平均模型的特征呈现;(3)基于尺寸归一化后同类型模型间对应标志点最优匹配的原则,实现三维下颌骨模型间的最优重叠,可最大程度体现关键标志点对重叠的作用。因此,本研究基于普氏分析算法计算的30例患者三维下颌骨数据的下颌骨平均模型,可较好体现同类型下颌骨关键特征的三维形态,并具有较好代表性。
3.3 模板法对下颌无显著畸形患者的三维下颌骨数据定点效果,可基本满足临床需求
非刚性配准算法是一种在不改变三角网格数量和三角网格关系的前提下,对模板三角网络模型(三维下颌骨模板)逐渐变形以逼近目标三维模型(患者下颌骨模型)的算法。本研究使用Meshmonk程序是一种效率较好的三维模板数据迭代变形算法,其特点表现在:曲率特征或形状位置特征显著的区域变形匹配效果较理想,标志点定点误差也较小,如本研究中的喙突顶点[(0.56±0.14) mm和(1.01±0.44) mm]、颏顶点(0.84±0.32) mm、下切牙点(0.72±0.39) mm、髁突最外侧点[(0.77±0.50) mm和(0.96±0.38) mm]等,均为曲率特征明显、位置特征显著的三维解剖标志点,定点误差在1 mm左右;曲率特征不显著区域,模板变形匹配缺少特征约束,标志点定点误差随之增大,如下颌升支前缘点[(2.57±1.10) mm和(2.52±0.95) mm]、下齿槽座点(2.33±1.06) mm、髁突顶点[(1.94±0.60) mm和(2.24±0.97) mm]等,定点误差在2 mm左右;总体上均可以满足临床需求[26]。
本研究基于构建的三维下颌骨平均形态模板和非刚性配准算法,实现了患者下颌骨三维数据的自动标志点确定,具有较好的灵活性和适应性,可根据口腔临床诊疗实际需求,灵活调整下颌骨模板标志点的数量和位置,无需改变算法程序,即可实现患者下颌骨定点的自动、灵活调整。口腔颅颌面解剖标志点的标注是口腔导航手术、口腔三维头影测量、颅颌面缺损数字化辅助重建手术等临床应用中诊断分析、虚拟设计的重要基础与前提。采用本研究所建立的方法应用于10例颅颌面无明显畸形患者的下颌骨数据,19个标志点的平均定点误差为(1.42±0.95) mm,与既往研究结果相比,标志点的定位精度有所提高,可初步满足临床医师的标志点标注需求。在本研究的基础上,后续可进一步对此方法的临床适用性进行探索研究,一方面可针对临床上不同层厚与分辨率的CT三维重建后的下颌骨数据采用本研究方法定点的精度差异展开研究,另一方面可针对临床中不同种类的下颌骨畸形患者,通过建立相应的三维下颌骨模板和改进非刚性配准算法对点约束限制的方式,进一步提高本方法定点的精度、扩展其适用范围。此外,还可将本研究的下颌骨解剖特征自动标注扩展至牙列标志点、上颌骨标志点的自动、精准标注中,以评价本方法学研究的临床适用性,相关研究有待后续开展。
参考文献
Mandibular reconstruction
[J].DOI:10.1016/j.oraloncology.2017.12.020 [本文引用: 1]
Contemporary reconstruction of the mandible
[J].DOI:10.1016/j.oraloncology.2009.11.006 [本文引用: 1]
点构法构建下颌骨正中矢状平面的初步探究
[J].DOI:10.3969/j.issn.1674-8115.2019.01.010 [本文引用: 1]
基于机器学习的颌骨特征点还原法辅助跨中线颌骨缺损重建
[J].DOI:10.19438/j.cjoms.2020.04.007 [本文引用: 1]
Predicting the premorbid shape of a diseased mandible
[J].
替牙期儿童下颌骨发育的三维特征
[J].DOI:10.3969/j.issn.2095-9400.2014.10.004 [本文引用: 1]
Automatic localization of three-dimensional cephalometric landmarks on CBCT images by extracting symmetry features of the skull
[J].DOI:10.1259/dmfr.20170054 [本文引用: 2]
Joint craniomaxillofacial bone segmentation and landmark digitization by context-guided fully convolutional networks
[J].
Context-guided fully convolu-tional networks for joint craniomaxillofacial bone segmentation and landmark digitization
[J].DOI:10.1016/j.media.2019.101621 [本文引用: 1]
MeshMonk: Open-source large-scale intensive 3D phenotyping
[J].DOI:10.1038/s41598-019-42533-y [本文引用: 2]
Procrustes methods in the statistical analysis of shape
[J].
基于三维人脸模板的颜面解剖标志点自动定点方法初探
[J].DOI:10.3760/cma.j.cn112144-20210913-00409 [本文引用: 1]
Comparison of three methods of facial measurement
[J].DOI:10.1016/j.ijom.2006.10.001 [本文引用: 1]
Image processing for craniofacial landmark identification and measurement: A review of photogrammetry and cephalo-metry
[J].DOI:10.1016/j.compmedimag.2004.06.002 [本文引用: 1]
Automated craniofacial landmarks detection on 3D image using geometry characteristics information
[J].
A coarse-to-fine approach for 3D facial landmarking by using deep feature fusion
[J].DOI:10.3390/sym10080308 [本文引用: 1]
Nasolabial shape and aesthetics in unilateral cleft lip and palate: An analysis of nasolabial shape using a mean 3D facial template
[J].DOI:10.1016/j.ijom.2020.06.003 [本文引用: 1]
A three-dimensional comparison of a morphometric and conventional cephalometric midsagittal planes for craniofacial asymmetry
[J].DOI:10.1007/s00784-011-0512-4 [本文引用: 1]
3D facial landmarks: Inter-operator variability of manual annotation
[J].DOI:10.1186/1471-2342-14-35 [本文引用: 1]